AQA A-Level 物理/原子结构
我们今天所知的原子,最初并非如此。正如你可能从 GCSE 物理中所知,原子的结构由原子核和电子组成。这并不完全是真相,但原子结构的布局有一些区别。为了更好地理解这一点,我们需要看看现代原子结构是如何被发现的。

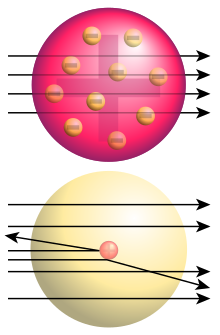
最初,原子被认为是一小块固体物质。人们知道原子是最小的东西;“原子”这个词来自希腊语,意思是不可分割的。所以如果原子是最小的东西,那么把它想象成一种固体果冻似乎很合理。
卢瑟福有不同的想法,为了验证他的想法,他必须制作一个非常薄的固体层。他使用金,因为金比其他任何材料更容易滚动或锤成薄固体层。他想要一层薄薄的,因为他想知道原子是否真的是固体。
为了验证他的想法,他向薄片发射了α粒子(通常写成 -粒子)。这些粒子由 2 个质子和 2 个中子组成,即氦原子核。它们很容易使用,因为一种常见的放射性衰变会发射 -粒子。当这项实验在 1909 年由卢瑟福的助手盖革和马斯登首次进行时,他们发现了一个相当有趣的结果。大多数粒子直接穿过了薄片。然而,其中有一些弹了回来。如果原子真的是一种果冻状固体,这种行为就无法解释。
如果我们思考一下这个结果,并在宏观尺度上考虑它,我们可以了解正在发生的事情。想象一下,我们有一个铁丝网,并且想象一下它非常坚固,我们向它发射球。让这个铁丝网成为我们经常遇到的那种网格,孔约 75 毫米见方。如果我们发射一个足球,我们并不奇怪它会直接弹回来。足球比铁丝网的孔洞大得多,因此铁丝网看起来是固体的。如果我们向铁丝网打高尔夫球,我们并不惊讶大多数球会直接穿过它,而那些正好击中铁丝的球会弹回来。如果我们用气枪发射弹丸,我们预计会有更多弹丸直接穿过它。
这种思考方式让卢瑟福对原子的结构有了想法。
- 他认为,因为大多数 -粒子直接穿过了原子一定包含大部分的空隙。
- 有些α粒子散射开,因此它们一定是被某种东西排斥了。
- 那种东西一定带正电荷才能排斥 -粒子的正电荷,而且它必须比 -粒子重才能让它弹回来。
这给了卢瑟福一个想法,即原子大多是空隙,有一个重的、带正电的原子核,而相对轻的、带负电的电子像行星绕恒星一样绕着它运行。(当然,在那个时代,我们只知道我们的太阳有行星。)
正如我们现在所知,原子包含
- 核子(质子和中子捆绑在一起)
- 电子
现在,关于原子需要记住的是原子是由原子核中质子的数量来定义的,所以如果原子核中有 1 个质子,那么它就是氢,因为它的原子序数(质子数)是 1。如果你想知道元素是什么,可以在元素周期表中查找。现在,这里有一些快速的事实
- 原子中的电子数量等于质子数量,因为 1 个质子的电荷吸引了 1 个电子(在 AS 中是这样的)
- 当电子从原子中移除或添加到原子中时,它就变成了离子。这被称为电离。
- 当原子核中中子的数量与通常情况不同时,原子就是同位素。
- 同位素具有相同的物理和化学性质,但原子核可以是稳定的或不稳定的,例如,C-12 和 C-14 都存在于物质中,但 C-14 同位素是不稳定的
这些都是重要的概念,因为它们是你在模块中后面学习的其他理论和模型的基础。现在,记住这些定义。
- 同位素是同一元素的原子,由于原子核中中子数量不同而具有不同的质量.
- 离子是电子数量与质子数量不同的原子,导致带电。
| A | X |
| Z |
| 4 | He |
| 2 |
为了理解这些符号的含义,你需要知道上面和下面的值代表什么。上面的值,
- A 是元素原子核中质子和中子的数量,称为核子数
- Z 是原子核中质子的数量,因此...
- 中子的数量。
现在,说了这么多,你需要能够计算这些粒子的质量和电荷,并且你需要使用它们的特定值,这与 GCSE 不同。别担心,你不需要记住它们,因为你会在试卷最前面得到一个数据表。说了这么多,记住它们也没坏事!
| 粒子 | 电荷 | 质量 |
| 质子 | ||
| 中子 | 无 | |
| 电子 |
练习题
[edit | edit source]不要被措辞吓倒,确保 **阅读并理解题目要求的答案,以及哪些部分只是解释**。要查看答案,请看下面。
- 钚-210 的一种同位素是一种放射性同位素,会发射α射线。计算:
- 质子的数量
- 电子的数量
- 中子的数量
- 该同位素经历电离过程,从原子中去除 4 个电子。计算原子的总电荷。
答案
[edit | edit source]- 质子数量 = 92,中子数量 = 116,电子数量 = 94
- (2 x 1.60 x10−19) = + 3.2 x10−19






