生物医学工程理论与实践/神经工程
另请参见 维基百科,神经工程.
神经工程是生物医学工程的一个学科,它利用工程技术来理解、修复、替代或增强神经系统。
神经工程是一个高度跨学科的领域,融合了神经科学、电子工程、临床神经学、材料科学、纳米技术、计算机工程等等。该领域的主要目标是更好地理解和模拟神经系统的功能和功能障碍,并设计出适当的增强和/或替代神经系统功能障碍的部分。
神经工程将广泛的工程和基础科学原理与广泛的生物学和医学科学结合在一起。它将基础和应用工程与科学研发与基础和应用神经科学联系起来。
古埃及人和罗马人使用电(以电鱼的形式)用于治疗目的。在 1790 年代,意大利医生路易吉·伽伐尼在用静电机的火花使青蛙肌肉抽搐时,证明了神经冲动的电气基础。[1]:67–71 科学界同行普遍接受了伽伐尼的观点;但亚历山德罗·伏特证明了电不是来自动物组织,而是来自金属(黄铜和铁)在潮湿环境中的接触。另一方面,在另一个实验中,伽伐尼通过用一只青蛙的神经触碰另一只青蛙的暴露肌肉来引起肌肉收缩。他首次证明了生物电存在于活组织中。吉约姆·杜申(1806 年 9 月 17 日,法国布洛涅-比扬库尔 - 1875 年 9 月 15 日,法国巴黎)恢复了伽伐尼的研究。他是第一个描述几种神经和肌肉疾病的人,并且在推进治疗这些疾病的方法方面,创造了电诊断和电疗法。
在 20 世纪中叶,电记录作为观察神经元功能的窗口变得流行起来

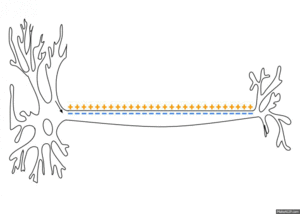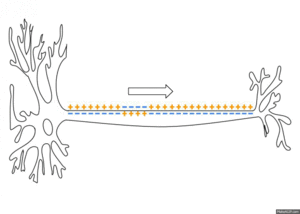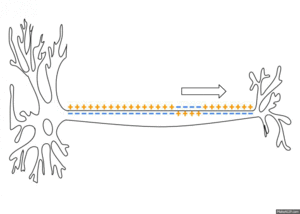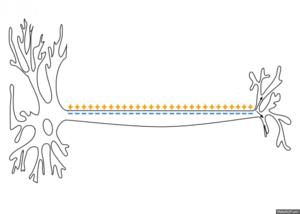
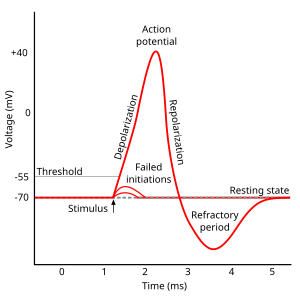
质膜内外不同电荷分布产生膜电位(也称为跨膜电位或膜电压)。建立和维持静息膜电位的两种力量是被动(通过通道扩散)和主动(钠钾泵)[2]。相对于神经元膜的胞质侧,静息电位的典型值范围为-70 到 -80 毫伏。与肌肉一样,神经元利用膜电位变化作为通信信号来接收、整合和发送信息。膜电位的差异可以由离子的渗透性和膜两侧的离子浓度产生。离子通道的开放和关闭可以引起静息电位的偏离。如果内部电压变得更负(例如,从 -70 毫伏到 -80 毫伏),则称为超极化;如果内部电压变得不太负(例如,从 -70 毫伏到 -60 毫伏),则称为去极化。在可兴奋细胞中,明显大的去极化会导致动作电位(长距离信号)。但是,离子浓度通常不会快速变化。因此,梯度电位是由神经元膜的被动电学特性造成的。
可兴奋膜之间存在细胞间通信。它们不会随着距离的增加而减弱,被称为“神经冲动”或“尖峰”。神经元产生的动作电位的时序称为其“尖峰序列”。刺激通过打开位于轴突上的特定电压调节门控通道来改变神经元膜的渗透性。轴突只能产生动作电位。
动作电位的产生(由去极化引起)遵循三个连续的变化
1. 钠离子通透性增加,膜电位相反。
2. 钠离子通透性降低。
3. 钾离子通透性增加,发生复极化。
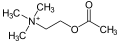
神经元树突中的电压脉冲具有不同的强度。神经元树突的刺激(由另一个神经元或作为特殊受体)会产生梯度电位。刺激可以通过多种方式发生,例如化学刺激(神经递质等)、机械刺激(某些疼痛感受器、毛发感受器等)、光刺激(光感受器)以及其他一些方式。无论如何,这些刺激都会带来相同的结果。树突上的某些受体蛋白离子通道被激活并打开。这会导致离子的流入(或流出)。根据进入(或离开)的离子,它会导致去极化(变得不那么负面,-70 到 -60mV,一种可能导致动作电位的兴奋性反应)或超极化(变得更负面,-70 到 -80mV,一种抑制性反应,使动作电位更难发生)。受体蛋白离子通道被刺激得越多,信号就越强或越强烈。对受体蛋白离子通道的轻微刺激通常会打开通道并接受离子。
然而,要使轴突起始段发生达到阈值的去极化,通常需要打开多个去极化受体蛋白离子通道。因此,梯度电位会累积。离子通道的总极化效应会加在一起。一个通道不能刺激动作电位,需要多个通道协同工作才能使膜去极化到足以引起动作电位的程度。梯度电位(或受体电位)是膜区域的短寿命去极化或超极化。这些变化会导致局部电流流动,这些电流流动会随着距离的增加而减弱。
梯度电位与刺激强度成正比,是刺激强度或强度的直接反映。刺激越强烈,打开的离子通道越多,电压变化(超极化或去极化)就越大,电流传播的距离就越远。
当离子涌入时会发生刺激极化。这些离子会聚集在受刺激区域附近。从那里,过量的离子会向各个方向辐射出去,极化相邻的膜。当这种极化像波浪一样传播时,它会在其身后留下一个曾经极化的膜的尾迹,该膜非常快地恢复到静息膜电位。
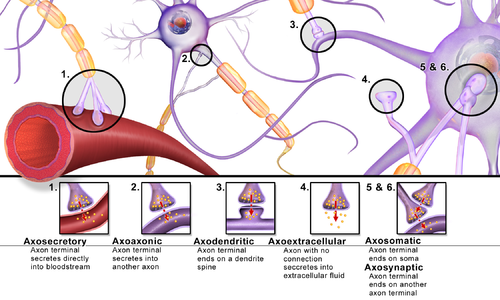
就像我们家里的电气系统中的电线一样,神经细胞以称为神经通路的形式相互连接。与我们家里的电线不同,神经细胞不会接触,而是在突触处彼此靠近。在突触处,两个神经细胞被突触间隙隔开。发送神经元称为突触前细胞,而接收神经元称为突触后细胞。神经细胞通过突触从突触前细胞传递到突触后细胞,以神经递质的形式发送化学信息,并且是单向的。
使用神经递质的突触传递过程如下
- 神经递质的合成和储存
- 神经递质释放
- 神经递质突触后受体
- 神经递质失活
在神经元中合成的神经递质分为两大类:**小分子神经递质**和**神经肽**。**小分子神经递质**在轴突末梢内合成(例如乙酰胆碱 (ACh))。这些分子合成所需的一些前体被选择性转运蛋白摄取到末梢膜上。其他是神经元内细胞过程的副产品,因此很容易获得。**神经肽**在大小和合成方式上都不同于小分子神经递质。神经肽的长度通常在 3 到 36 个氨基酸之间。因此,它们比小分子神经递质更大。由于它们需要简单的酶促反应,因此小神经递质在轴突末梢内产生,而神经肽在细胞体中产生,因为它们的合成需要肽键形成。神经肽的合成类似于细胞内任何分泌蛋白的过程。首先,在细胞核内,发生特定肽编码序列的 DNA 基因转录,它用作模板构建相应的信使 RNA 链。mRNA 然后移动到核糖体,在那里开始翻译过程。在翻译过程中,mRNA 的序列充当代码,将相应的氨基酸序列串在一起,这些氨基酸序列将成为末梢处所需的神经肽。在该分子可以被运输到末梢并释放到突触间隙之前,它必须在内质网 (ER) 中进行加工,在高尔基体中进行包装,并在储存囊泡中沿轴突运输到末梢。
一旦合成,小分子和神经肽类神经递质都储存在轴突末梢内的囊泡中,直到动作电位到达并释放它们。大多数小分子神经递质储存在直径为 40~60 纳米的微小囊泡中。储存神经肽的囊泡更大,直径在 90 到 250 纳米之间。
含有神经递质的囊泡储存在神经元的末梢,在**活性区**或活性区附近。这些囊泡通过对肌动蛋白丝、微管和细胞骨架的各种成分进行结合的 Ca2+敏感囊泡膜蛋白固定在适当位置。当动作电位到达突触前神经元的末梢时,突触前膜中的电压依赖性钙 (Ca2+) 通道打开,Ca2+ 涌入。这种钙离子流入会触发一系列事件,最终将神经递质从储存囊泡中释放到突触间隙。
释放到突触间隙后,神经递质会与突触后细胞膜上的受体蛋白进行交流,导致膜上的离子通道打开或关闭。当这些通道打开时,会发生去极化,涉及另一个动作电位的启动。识别神经递质的突触后受体有两种类型:称为配体门控离子通道的离子型受体和称为 G 蛋白偶联受体的代谢型受体。
在突触后受体识别神经递质分子后,它会被释放回突触间隙。一旦进入突触,它必须被化学失活或快速去除,以避免对突触后细胞的持续刺激和动作电位的过度放电。
-
乙酰胆碱代谢
-
儿茶酚胺和痕量胺生物合成
-
GABA 能突触
神经递质是大脑化学物质,在整个大脑和身体中传递信息。神经元之间信息的传递是通过神经递质跨越称为突触的小间隙运动来实现的。神经递质从突触前神经末梢的一个神经元释放。神经递质剂包括激动剂、拮抗剂、降解抑制剂、摄取抑制剂、消耗剂、前体以及受体功能的调节剂[3]。神经递质可分为氨基酸、肽类和单胺类。
- 小分子神经递质物质:乙酰胆碱 (ACh)、多巴胺 (DA)、去甲肾上腺素 (NE)、血清素 (5-HT)、组胺、肾上腺素、氨基酸、γ-氨基丁酸 (GABA)、甘氨酸、谷氨酸、天冬氨酸
- 神经活性肽(部分列表):缓激肽、β-内啡肽、脑啡肽、降钙素、胆囊收缩素、脑啡肽、强啡肽、胰岛素、胃泌素、P物质、神经降压素、胰高血糖素、促胰液素、生长抑素、胃动素、加压素、催产素、催乳素、促甲状腺激素、血管紧张素 II
- 睡眠肽:加拉宁、促甲状腺激素释放激素、促性腺激素释放激素、生长激素释放激素、促黄体生成素、血管活性肠肽
- 可溶性气体:一氧化氮 (NO)、一氧化碳
表: 选定的神经递质及其功能
工作原理
[edit | edit source]神经调节和神经增强
[edit | edit source]神经调节被国际神经调节学会定义为“通过向身体的目标部位传递电刺激或化学物质来改变神经活动”。它是为了使神经功能正常化或调节而进行的。神经调节是神经系统中多种神经递质控制各种神经元群体(一个神经元使用不同的神经递质连接到多个神经元)的过程。神经调节可能涉及电磁刺激,例如强磁场重复经颅磁刺激、非常小的电流或可能是光遗传学。[4]神经调节使用医疗设备技术来增强或抑制神经系统的活动,以治疗疾病。这些技术包含可植入的和不可植入的设备,这些设备传递电气、化学或其他物质,以可逆地改变大脑和神经细胞的活动。[4]
神经肌肉电刺激 (NMES)
[edit | edit source]神经肌肉电刺激可以广泛地分为功能性或治疗性。治疗性神经肌肉刺激是指使用刺激瘫痪的肌肉来最大程度地减少特定的损害,如运动无力、痉挛、活动范围受限和心血管衰竭。功能性神经肌肉刺激 (FNS)是指使用刺激以精确的顺序激活瘫痪的肌肉,以帮助完成日常生活活动 (ADL) 或为关节提供稳定性,以维持原始的生物力学特性和功能。提供 FNS 的设备或系统被称为神经假体。[5]
神经再生
[edit | edit source]
神经再生是指神经组织、细胞或细胞产物的再生或修复[6]。再生过程中发生的步骤可以分为以下主要事件:瓦勒氏变性、轴突再生/生长和神经再支配[7]。从其他角度看,神经再生包含神经发生、神经可塑性和神经修复——将活细胞作为治疗方法进行移植[8]。考虑到范围和速度,周围神经系统 (PNS) 和中枢神经系统 (CNS) 的神经再生机制非常不同。
周围神经系统再生
[edit | edit source]周围神经损伤根据对神经和周围结缔组织的损伤程度在 Seddon 分类中进行分类[9]。神经损伤的最低程度,即暂时中断传导,而没有轴突连续性损失,称为神经传导阻滞[10]。第二种程度称为轴突断裂,与轴突及其髓鞘覆盖层的相对连续性丧失有关,但它保留了神经的结缔组织框架(包囊组织、外鞘和内鞘得到保留)。[11]。最后一种程度称为神经断裂,是整个神经纤维的完全断裂或破坏[12]。
与中枢神经系统不同,周围神经系统可以再生[13]。瓦勒氏变性发生在神经再生之前。在瓦勒氏变性期间,雪旺细胞和巨噬细胞相互作用以从远端损伤部位去除髓鞘和受损的轴突。当无神经支配的雪旺细胞增殖并且剩余的结缔组织基底膜形成内鞘管时,形成班氏带。班氏带对于引导再生轴突很重要[14]。
在神经元胞体处,发生色溶现象,其中细胞核移动到胞体的周边,内质网破裂并分散。神经损伤改变了细胞的代谢功能。该细胞试图产生用于生长和修复的分子,而不是产生用于突触传递的分子。这些因素包括 GAP-43、微管蛋白和肌动蛋白。当细胞准备好进行轴突再生时,色溶现象会逆转[15]。
轴突再生以生长锥的形成为特征[16]。生长锥位于称为轴突和树突的结构上的神经细胞的最尖端。它们包括肌动蛋白丝 (F-肌动蛋白) 的束,这些丝为它们提供了形状和支撑。生长锥与雪旺细胞产生的分子(如层粘连蛋白和纤连蛋白)相互作用[14]。
与周围神经系统再生不同,中枢神经系统再生不会伴随广泛的再生。它受到神经胶质细胞和细胞外环境的抑制性影响的限制。中枢神经系统 (CNS) 的再生是可能的,新的神经元,由内源性干/祖细胞增殖或外源性干/祖细胞(具有替代丢失组织的潜力)的给药下生成,将分化、存活并整合到现有的神经网络中,以及轴突再生[17]。由于一些研究报道了成人神经干细胞的存在[18][19][20],基于神经组织工程的神经可塑性和神经干细胞的概念导致了神经修复作为 CNS 神经退行性疾病替代疗法的想法[17] [21] 。
神经影像包含各种技术,可以直接或间接成像神经系统的结构、功能/药理学。它是医学、神经科学和心理学中一个相对较新的领域[22]。专门从事临床环境中神经影像的执行和解释的医生是神经放射科医生。
神经影像分为两类
- 结构影像,涉及神经系统的结构和对大体积 (大尺度)颅内疾病(如肿瘤)和损伤的诊断。
- 功能影像用于诊断更精细尺度 (例如阿尔茨海默病) 的代谢性疾病和病变,以及用于神经学和认知心理学研究以及构建脑机接口。
另请参阅 人工神经网络
神经网络(人工神经网络:ANN)是一种信息处理范式,其灵感来自动物中枢神经系统(如大脑)处理信息的方式。这种范式的关键要素是信息处理系统的独特结构。它由大量高度互连的神经元组成,这些神经元可以计算输入值。第一个人工神经元是由神经生理学家沃伦·麦卡洛克和逻辑学家沃尔特·皮茨于 1943 年开发的[23]。许多重要的研究得到了廉价的计算机模拟的推动。在马文·明斯基和西摩尔·派珀特发表机器学习研究之后,神经网络研究放缓[24] (1969)。他们发现了处理神经网络的计算机器的两个关键问题。第一个问题是单层神经网络无法处理异或电路。第二个问题是计算机不够复杂,无法有效地处理大型神经网络所需的长时间运行。直到计算机拥有更大的处理能力,神经网络研究才有所放缓。另一个关键的后期进展是反向传播算法,它有效地解决了异或问题 (Werbos 1975)[25]。

人工神经元是一个数学函数,作为生物神经元的模型。人工神经元是人工神经网络中的组成单元。对于给定的人工神经元,假设有m + 1 个输入,具有信号x0 到xm 和权重w0 到wm。通常,x0 输入将是值 +1,这使其成为wk0 = bk 的偏差输入。这仅留下了m 个实际输入到神经元:从x1 到xm。
kth 神经元的输出是
其中 (phi) 是传递函数[26]。输出类似于生物神经元的轴突,其值通过突触传播到下一层的输入。它也可以作为输出向量的一部分退出系统。其传递函数权重是计算出来的,阈值是预先确定的。局限性在于简单的类神经网络,例如 McCulloch-Pitts 模型,有时被表达为“卡通模型”,因为它们试图反映一个或多个神经生理学观察结果,但不考虑真实性。 [27]
神经接口
[edit | edit source]神经接口系统通过刺激或记录神经组织,在神经系统和外部世界之间提供直接的通信途径,以帮助患有感觉、运动或其他神经功能障碍的人。这些研究被称为实验神经科学的一个新分支,被称为脑机接口 (BMI)、脑机接口 (BCI)、神经假体或神经接口系统 (NIS)。每个设备中的电子封装激活一组微小的电极,这些电极与身体中的健康神经元接触。电极发出的信号绕过大脑或神经系统受损的区域,以恢复功能、阻断疼痛或预防癫痫发作。尽管电刺激系统已广泛用于临床应用,但记录和破译神经信号的神经接口才刚刚开始用于临床系统,以帮助有残疾的人。成功的 神经接口示例包括人工耳蜗[28][29],它为重度听力障碍的人提供声音感,以及深部脑刺激器 (DBS) [30],它有助于预防癫痫患者和帕金森病患者的癫痫发作。
自 1990 年代后期以来,神经接口研究在使用神经元尖峰的闭环控制的基础上取得了显著发展。Chapin 及其同事展示了一只大鼠通过从感觉运动皮层的多电极记录控制一维进食器的能力[31]。此后,大量研究(Carmena 等人,2003 [32]、Musallam 等人,2004 [33]、Santhanam 等人,2006 [34]、Taylor 等人,2002 [35] 等)证明了灵长类动物的闭环控制是可行的。常见的闭环神经接口系统由四个部分组成:(1)提取神经信号的记录阵列,(2)将这些神经信号转换为一组命令信号的解码算法,(3)由这些命令信号控制的输出设备,以及(4)以视觉和潜在的其他感觉方式进行的感觉反馈。
神经植入物必须设计得尽可能小,以便在靠近大脑、眼睛或耳蜗的特定区域进行微创手术。这些植入物通过无线方式与其假体对应物通信。此外,目前通过皮肤的无线能量传输来接收能量。通常,植入物附近的组织对温度升高非常敏感。这意味着功耗必须最小,以避免组织损伤。 [36]

输入电极
[edit | edit source]

颅内电极由植入在聚合物或硅上的导电电极阵列组成,或者由一根带有一个暴露的尖端和绝缘层的导线电极组成,该绝缘层用于不需要刺激或记录的部分。
目前的可植入微电极无法根据慢性尺度记录单单元或多单元活动。Lebedev 和 Nicolelis 回顾了该领域真正改进技术以达到临床实施水平的具体需求。简而言之,他们评论中的 4 个要求是
硬件
[edit | edit source]芯片已在芯片上整合了不同程度的数据压缩[39],包括尖峰排序(Chae 等人,2009 年)。虽然许多系统功耗过高,无法从电池植入物供电,但 Sarpeshkar 等人已经制造了放大器和模数转换器,其功耗低于每 20 ksps 通道 9 uW[40]。虽然可用集成电路的小面积和低功耗足以处理大部分神经数据通道,但仍需解决一些问题。例如,植入物可以在体内停留多长时间?涂有 6 um 聚酰亚胺 C 的电子设备已被证明可以工作长达 276 天[41]。Plexon、Tucker Davis、NeuroLynx 等商业系统依赖于密封在焊接钛外壳中的密封式馈通连接器,电子设备位于其中。但是,使用数百个电极和高密度微型密封式馈通的脑机接口尚不存在。
解码器流程
[edit | edit source]性能评估
[edit | edit source]神经机器人学
[edit | edit source]神经机器人学是神经科学与机器人学的一部分,涉及对像大脑启发算法这样的具身自主神经系统科学和技术的学习和应用。神经机器人学从“大脑是具身的,身体是嵌入环境中的”这一理念出发。模拟环境可能会对模型产生无意的偏差。此外,真实环境是不可预测的、多模式的和嘈杂的;这种环境的人工设计很难模拟。因此,大多数神经机器人需要与现实世界互动,而不是模拟环境。 [42]

存在许多类别的神经生物学启发机器人设备。三种常见的神经机器人用于研究运动控制、记忆和动作选择。
- 运动控制和运动
- 学习和记忆系统
- 价值系统和动作选择
运动控制和运动
[edit | edit source]神经机器人已被证明对研究动物运动和运动控制以及开发机器人控制器非常有效。机器人的运动控制是根据运动系统作用机制的一系列神经启发理论设计的。中枢模式发生器的神经模型,即能够驱动重复行为的运动神经元簇,已被用于脊椎动物腿式运动,例如四足行走机器人 [43] [44]。另一种运动控制方法是使用预测控制器将笨拙、容易出错的运动转化为平滑、准确的运动。利用这些想法,设计的机器人可以避开障碍物 [45][46],产生准确的视觉 [47] 以及生成自适应手臂运动 [48][49][50]。
学习和记忆系统
[edit | edit source]设计用于测试动物记忆系统理论的机器人。目前,许多研究都集中在大鼠的记忆系统,即海马体,研究定位细胞,这些细胞在特定已学习的空间位置会特异性地放电。 [51][52]
价值系统和动作选择
[edit | edit source]动作选择研究涉及对动作及其结果的负面或正面反馈。大脑中此类研究的例子包括多巴胺能、胆碱能和去甲肾上腺素能系统,这些系统中的神经递质,如多巴胺或乙酰胆碱,会对有益的神经信号进行正向强化。 [53][54][55]。一项关于这种相互作用的研究涉及达尔文 VII 机器人,它使用视觉、听觉和模拟味觉输入来“食用”导电金属块。随机选择的好的金属块上有条纹图案,而坏的金属块上有圆形图案。味觉感是通过金属块的导电性模拟的。Doya 的团队一直在研究“赛博老鼠”中多种神经调节剂的影响,例如在环境中自主移动的两轮机器人。 [56]。这些机器人可以为了自我保护和自我复制而移动,例如搜索地板上的电池组并为其充电,然后通过其红外通信端口将此信息传达给其他机器人。包括研究多巴胺等神经调节剂如何影响决策,神经机器人学家一直在研究基底神经节作为调解动作选择的模型。 [57]。Prescott 及其同事在一个机器人中嵌入了一个基底神经节模型,该机器人必须从依赖于环境的几个动作中进行选择。
神经组织再生
[edit | edit source]外周神经系统的手术连接
[edit | edit source]在外周神经系统中,如果损伤较小,神经可以自行再生。然而,对于像近端和远端神经末端之间的小间隙,可以通过手术重新连接断裂的神经,将神经的两端缝合在一起。缝合神经时,神经的每个束都会重新连接,将神经连接起来。这种方法不适用于较长距离的间隙,因为神经末端需要保持张力。这种张力会阻断神经再生。 [58]
外周神经系统的组织移植
[edit | edit source]组织移植使用神经或其他材料来桥接断裂神经的两端。组织移植分为自体组织移植、异体组织移植和无细胞移植。自体组织移植是指将同一身体的不同部位的组织转移到另一个部位。 [59]。这些自体神经移植是目前外周神经移植的标准,因为它具有高度的生物相容性,但也存在一些问题,例如从患者身上获取神经以及为将来使用而储存大量自体移植。异体组织移植和无细胞移植(含有基于 ECM 的材料)是指不来自患者的组织,而是可以从尸体或动物身上获取。由于它们不来自患者,因此很容易获得,但这些组织在潜在的疾病传播方面存在一些困难。目前,正在研究提高异体组织移植功效的方法。 [58]
神经引导通道
[edit | edit source]
与自体移植相比,神经引导导管是一种人工引导轴突再生以帮助神经再生的方法,是神经损伤的临床治疗方法之一。由于供体组织的有限性和自体移植中的功能恢复,神经组织工程研究已将重点放在生物人工神经引导导管上,作为替代疗法。类似的技术也正在研究用于脊髓神经修复,但中枢神经系统的神经再生会面临挑战,因为其轴突在其原生环境中不会再生。 [60] 引导方法可以减少神经的瘢痕形成,从而提高神经在重新连接后传递动作电位的功能。在这种方法中,使用了两种类型的材料:天然材料和合成材料。
生物材料通常具有良好的生物相容性,并且可以很容易地降解,因为它来自自然界。然而,不幸的是,它在控制机械性能和降解速率方面存在局限性。此外,天然材料始终有可能引起免疫反应或含有微生物。 [61]。在天然材料的生产过程中,大规模纯化过程会产生意想不到的结果。 [62] 困扰天然聚合物的一些其他问题是,由于可能发生塌陷、瘢痕形成和早期重新吸收,它们无法支撑跨越长病变间隙的生长。 [62] 具有促进神经修复潜力的生物材料包括聚唾液酸(PSA)、胶原蛋白、蜘蛛丝纤维、蚕丝丝素蛋白、壳聚糖、文石、海藻酸盐、透明质酸、糖胺聚糖、层粘连蛋白、壳聚糖等。
合成材料也为组织再生提供另一种方法。合成聚合物可能是不可降解的或可降解的。但是,对于神经组织工程,更倾向于使用可降解材料,因为长期影响(如炎症和瘢痕)会损害神经功能。可以根据目的控制聚合物的机械性能和降解速率,并且消除了对免疫原性的担忧。 [61] 目前,许多不同的合成材料正在神经组织工程中使用。但是,问题在于这些材料缺乏生物相容性和生物活性。这意味着这些聚合物并不完美,不能促进细胞附着、增殖和分化。 [63] 目前,研究最常用的材料主要集中在可生物降解的聚酯上,例如聚乳酸、聚乙醇酸、聚己内酯、聚乙二醇(FDA 批准)的共聚物或共混物,可生物降解的聚氨酯、其他聚合物以及可生物降解的玻璃也在研究中。合成材料的其他潜力包括导电聚合物和生物修饰聚合物,以促进细胞轴突生长并维持轴突通道。 [58]

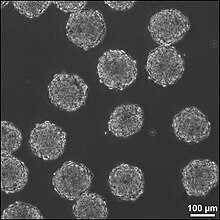
可以在体外人工创建组织,然后将其移植到损伤部位。这种方法可以治疗具有较大空腔的损伤,这些损伤需要大量的神经组织进行替换和再生。神经组织可以在体外用神经干细胞或祖细胞在 3D 支架中生长,形成胚状体 (EBs)。这些 EBs 由干细胞球体组成,其中内部细胞是未分化的神经细胞,周围细胞则分化程度更高。3D 支架用于将组织移植到损伤部位并构建人工组织和脑组织之间的合适界面。支架应该是可生物降解的并且具有生物相容性。它需要适合损伤部位,靠近现有组织并支持生长中的细胞和组织。结合使用干细胞和支架可以提高干细胞在损伤部位的存活率,从而提高治疗的有效性。[64]
表。支架的制备
| 支架的制备 | 特性 |
|---|---|
| CAD/CAM 技术 | 示例 |
| 静电纺丝 | 示例 |
| 乳化/冷冻干燥 | 示例 |
| 气体发泡 | 示例 |
| 纳米纤维自组装 | 示例 |
| 纺织技术 | 示例 |
| 热诱导相分离 (TIPS) | 示例 |
| 纳米纤维自组装 | 示例 |

增强神经组织再生的分子,包括药物、称为形态发生的生长因子和 miRNA,也可以直接注射到受损的 CNS 组织的损伤部位。脑部药物递送策略可以广泛地分为侵入性(基于神经外科)、药理学或生理学。基于神经外科的策略包括脑室内药物输注、脑内植入物和 BBB 破坏。基于药理学的策略包括使用微球、纳米球等颗粒,这些颗粒可以通过乳化、喷雾干燥、分散等方法制备。 [65][66]

神经增强或人类增强可用于治疗疾病和残疾,也可用于增强人类特征和能力。[68] 在某些圈子里,"人类增强技术"与新兴技术或融合技术或超人类主义同义。[69] 从其他观点来看,"人类增强"与人类基因工程大致同义,[70][71] 它通常是指将纳米技术、生物技术、信息技术和认知科学 (NBIC) 相结合以改善人类生活的普遍应用。[69] 深部脑刺激已被证明可以为目前使用这种疗法治疗帕金森病、原发性震颤、肌张力障碍、慢性疼痛、重度抑郁症和强迫症的患者提供治疗益处。[72] 人类增强带来的伦理问题是神经工程师在开发技术时需要解决的问题。一些有争议的想法是,人类增强可以维持或修改他们自己的思想和身体。[73] 此外,人们担心,一些增强会为那些能够并愿意使用它们的人创造不公平的身体或精神优势,并会加剧"有"和"无"之间的差距。 [74][75][76][77] 但是,一些支持者提倡"人类增强技术",并更喜欢用"赋能"来代替"增强"。[78] 他们试图为这些技术的独立安全测试辩护和发展,并为这些技术提供负担得起、普遍的获取途径。[79]

深部脑刺激 (DBS) 是一种神经外科手术,它将一种称为脑起搏器的微型医疗器械植入体内,该器械通过植入的电极向大脑特定区域发送电脉冲,用于治疗运动障碍和情感障碍。美国食品药品监督管理局 (FDA) 于 2002 年批准 DBS 作为治疗帕金森病的疗法,[80] 2003 年批准治疗肌张力障碍,[81] 2009 年批准治疗强迫症 (OCD)。[82] DBS 也被用于治疗各种情感障碍,包括重度抑郁症,但这些 DBS 应用尚未获得 FDA 批准。
深部脑刺激系统由三个部分组成:植入式脉冲发生器 (IPG)、导线和延长线。IPG 是一种由电池供电的神经刺激器,封装在钛外壳内,它向大脑发送电脉冲以干扰目标部位的神经活动。导线 是一种盘绕的金属线,由聚氨酯等生物相容性但不可降解的聚合物绝缘,带有四个铂或铱电极,并放置在大脑的一个或两个不同核团中。导线通过延长线连接到 IPG。它是一根绝缘线,从头部下方穿过皮肤,沿着颈部侧面,耳后到达 IPG,IPG 被放置在锁骨下方或某些情况下放置在腹部。[83] 导线放置在大脑中的位置取决于要解决的症状类型。IPG 可以由神经科医生、护士或经过培训的技术人员校准。[84]
所有这三个部分都通过手术植入大脑。导线植入可能需要局部麻醉或全身麻醉("睡眠 DBS")。在头骨中钻一个直径约 14 毫米的孔,并插入探针电极。在使用局部麻醉的清醒手术过程中,患者的反馈决定了永久电极的最佳放置位置。在睡眠手术过程中,术中 MRI 指导用于确定电极的位置。 [85] 通常,IPG 和延长线在全身麻醉下安装。[86]
- Bronzino, Joseph D. (2006 年 4 月)。生物医学工程手册,第三版. [CRC 出版社]. ISBN 978-0-8493-2124-5.
- Villafane,Carlos,CBET。(2009 年 6 月)。生物医学:从学生的角度,第一版。[Techniciansfriend.com]。 ISBN 978-1-61539-663-4.
{{cite book}}: CS1 maint: 多个名字:作者列表 (link)
- ↑ Whittaker,E. T. (1951),以太和电的理论史。第 1 卷,Nelson,伦敦
- ↑ Franco R, Bortner CD, Cidlowski JA (2006 年 1 月)。“电基因离子转运和质膜去极化在凋亡中的潜在作用”。J. Membr. Biol. 209 (1): 43–58。 doi:10.1007/s00232-005-0837-5。 PMID 16685600.
{{cite journal}}: CS1 maint: 多个名字:作者列表 (link) - ↑ 美国国立医学图书馆 - 医学主题词,神经递质
- ↑ a b “国际神经调节学会主页”. 检索于 2013 年 10 月 1 日.
- ↑ Joel A. DeLisa, Bruce M. Gans, Nicholas E. Walsh (2005),物理医学与康复:原理与实践,Lippincot Williams & Wilkins,第 1405 页
- ↑ 维基百科,神经再生
- ↑ 创伤和沃勒变性
- ↑ Enciu AM 等人。神经退行性疾病中的神经再生,BMC 神经学 2011,11:75
- ↑ “周围神经损伤”.
- ↑ Otto D. Payton & Richard P. Di Fabio 等人。物理治疗手册。丘吉尔·利文斯通公司。 ISBN 0-443-08499-8
- ↑ “神经损伤分类”.
- ↑ Otto D. Payton & Richard P. Di Fabio 等人。物理治疗手册。丘吉尔·利文斯通公司。 第 24 页。 ISBN 0-443-08499-8
- ↑ Fenrich,Keith;Gordon,Tessa (2004)。“周围神经系统和中枢神经系统中的轴突再生 - 当前问题和进展”。加拿大神经科学杂志。31 (2): 142–156。 ISSN 0317-1671.
- ↑ a b Campbell,William W. (2008 年 8 月 31 日)。“周围神经损伤的评估和管理”。临床神经生理学。119 (9): 1951–1965。 doi:10.1016/j.clinph.2008.03.018。 PMID 18482862.
- ↑ Burnett,Mark G.;Zager,Eric L. (2004)。“周围神经损伤的病理生理学:简要回顾”。Medscape Today:神经外科重点。 ISSN 1092-0684. 检索于 2013 年 8 月 11 日.
- ↑ Yoo,S (2010)。“轴突 mRNA 转运的动力学及其对周围神经再生的意义”。实验神经学。1. 223: 19-27。 doi:10.1016/j.expneurol.2009.08.011。 PMC 2849851. 检索于 2014 年 4 月 1 日.
{{cite journal}}: 未知参数|coauthors=被忽略 (|author=建议) (help) - ↑ a b Johansson BB:大脑和脊髓的再生和可塑性。J Cereb Blood Flow Metab 2007,27:1417-1430
- ↑ McKay R:中枢神经系统中的干细胞。Science 1997,276:66-71。
- ↑ Morshead CM,Reynolds BA,Craig CG,McBurney MW,Staines WA,Morassutti D,Weiss S,van der Kooy D:成年哺乳动物前脑中的神经干细胞:脑室下区细胞的相对静止亚群。Neuron 1994,13:1071-1082。
- ↑ Shihabuddin LS,Palmer TD,Gage FH:寻找神经祖细胞:治疗神经退行性疾病的前景。Mol Med Today 1999,5:474-480
- ↑ D. Kacy Cullen 等人,神经组织工程学用于神经再生和生物混合界面微系统体内研究(第二部分),生物医学工程关键评论,第 39 卷,2011 年第 3 期,第 241-259 页
- ↑ Filler, Aaron (2009 年 7 月 12 日)。“计算机影像在神经疾病诊断和神经外科中的历史、发展和影响:CT、MRI 和 DTI”。《自然预印本》。doi:10.1038/npre.2009.3267.4.
- ↑ McCulloch,Warren;Walter Pitts(1943)。“神经活动中固有思想的逻辑演算”。《数学生物物理学报》。5(4):115–133。doi:10.1007/BF02478259.
- ↑ Minsky,M.;S. Papert(1969)。《计算几何导论》。麻省理工学院出版社。ISBN 0-262-63022-2.
- ↑ Werbos,P.J.(1975)。《超越回归:行为科学预测和分析的新工具》。
- ↑ 维基百科,人工神经元
- ↑ F. C. Hoppensteadt 和 E. M. Izhikevich(1997)。《弱连接神经网络》。施普林格。第 4 页。ISBN 978-0-387-94948-2.
- ↑ Gifford RH, Shallop JK, Peterson AM。语音识别材料和天花板效应:对人工耳蜗植入计划的考虑。听力学和神经耳鼻喉科。2008;13:193–205.
- ↑ Wilson BS, Dorman MF。人工耳蜗:光辉的过去和灿烂的未来。听力研究。2008;242:3–21.
- ↑ Arle JE, Alterman RL。帕金森病的外科手术选择。北美医学临床。1999;83:483–98. vii.
- ↑ Chapin JK, Moxon KA, Markowitz RS, Nicolelis MA。使用运动皮层中同时记录的神经元实时控制机械臂。自然神经科学。1999;2:664–70.
- ↑ Carmena JM, Lebedev MA, Crist RE, O'Doherty JE, Santucci DM 等。学习通过脑机接口控制灵长类动物的伸手和抓取。公共科学图书馆生物学。2003;1:1–16.
- ↑ Musallam S, Corneil BD, Greger B, Scherberger H, Andersen RA。神经假肢的认知控制信号。科学。2004;305:258–62.
- ↑ Santhanam G, Ryu SI, Yu BM, Afshar A, Shenoy KV。高性能脑机接口。自然。2006;442:195–98.
- ↑ Taylor DM, Tillery SI, Schwartz AB。三维神经假肢装置的直接皮层控制。科学。2002;296:1829–32.
- ↑ Daniel Garrison。"最小化体内体传感器热效应". 检索于 2010 年 5 月 5 日.
- ↑ Lebedev, M.A., 脑机接口:过去、现在和未来。神经科学趋势,2006。29(9): p. 11.
- ↑ Nicolelis, M.A.L., 重构印记:同步、多位点、多单神经元记录。神经元,1997。18: p. 9.
- ↑ O'Driscoll, S.;Meng, T.H.;Shenoy, K.V. 和 Kemere, C.(2006)。神经元到硅:可植入假肢处理器 IEEE ISSCC(谈话):552-553。
- ↑ Sarpeshkar, R. 等人。(2008)。用于脑机接口的低功耗电路 IEEE Trans BioCAS 2(3): 173-183
- ↑ Sharma, A. 等人。(2011)。基于犹他州斜坡电极阵列的全集成无线神经接口的长期体外功能稳定性和记录寿命 J. Neural Eng. 8: 1-7
- ↑ Chiel, H. J., & Beer, R. D. (1997). 大脑拥有身体:适应性行为源于神经系统、身体和环境的相互作用。[社论材料]。神经科学趋势,20(12),553-557。
- ↑ Ijspeert, A. J., Crespi, A., Ryczko, D., 和 Cabelguen, J. M. (2007). 从游泳到行走:由脊髓模型驱动的蝾螈机器人。科学 315, 1416-1420。
- ↑ Kimura, H., Fukuoka, Y., 和 Cohen, A. H. (2007). 受生物启发的四足机器人的适应性行走。Philos Transact A Math Phys Eng Sci 365, 153-170
- ↑ McKinstry, J. L., Edelman, G. M., 和 Krichmar, J. L. (2006). 预测运动控制的小脑模型在基于大脑的设备中得到验证。美国国家科学院院刊 103, 3387-3392
- ↑ Porr, B., 和 Worgotter, F. (2003). 各向同性序列顺序学习。神经计算 15, 831-864
- ↑ Dean, P., Mayhew, J. E., Thacker, N., 和 Langdon, P. M. (1991). 模拟机器人摄像机-头部系统中的扫视控制:用于高效学习逆运动学的网络结构。生物控制论 66, 27-36
- ↑ Dean, P., Mayhew, J. E., Thacker, N., 和 Langdon, P. M. (1991). 模拟机器人摄像机-头部系统中的扫视控制:用于高效学习逆运动学的网络结构。生物控制论 66, 27-36
- ↑ Eskiizmirliler, S., Forestier, N., Tondu, B., 和 Darlot, C. (2002). 应用于由 McKibben 人工肌肉驱动的单关节机器人手臂控制的小脑通路模型。生物控制论 86, 379-394
- ↑ Hofstotter, C., Mintz, M., 和 Verschure, P. F. (2002). 小脑在行动:模拟和机器人研究。欧洲神经科学杂志 16, 1361-1376。
- ↑ O'Keefe, J., 和 Nadel, L. (1978). 海马体作为认知地图(牛津:克拉伦登出版社)。
- ↑ Mataric, M. J. (1998). 基于行为的机器人学作为合成人工行为和分析自然行为的工具。[回顾]。认知科学趋势,2(3),82-87。
- ↑ Aston-Jones, G., 和 Bloom, F. E. (1981). 行为大鼠中含有去甲肾上腺素的蓝斑神经元对非有害环境刺激表现出明显的反应。J Neurosci 1, 887-900
- ↑ Hasselmo, M. E., Hay, J., Ilyn, M., 和 Gorchetchnikov, A. (2002). 神经调节、θ 节律和大鼠空间导航。神经网络 15, 689-707
- ↑ Schultz, W., Dayan, P., 和 Montague, P. R. (1997). 预测和奖励的神经基础。科学 275, 1593-1599。
- ↑ Doya, K., 和 Uchibe, E. (2005). 网络啮齿动物项目:探索自我保护和自我复制的适应机制。适应性行为 13, 149 - 160。
- ↑ Prescott, T. J.,Montes Gonzalez, F. M.,Gurney, K.,Humphries, M. D. 和 Redgrave, P.(2006)。基底神经节的机器人模型:行为和内在处理。神经网络 19,31-61
- ↑ a b c Schmidt,Christine;Jennie Leach(2003 年 6 月)。“神经组织工程:修复和再生的策略”。《生物医学工程年度评论》。5:293-347。
- ↑ 免费词典,自体移植
- ↑ Schmidt,C. E.;Leach,J. B.(2003 年 8 月)。“神经组织工程:修复和再生的策略”。《生物医学工程年度评论》。5:293-347。doi:10.1146/annurev.bioeng.5.011303.120731。PMID 14527315。
- ↑ a b Lavik,E.;Langer,R.(2004 年 7 月)。“组织工程:现状和展望”。《应用微生物生物技术》。65(1):1-8。doi:10.1007/s00253-004-1580-z。PMID 15221227。
- ↑ a b Cai,J.(2005 年 11 月)。“含有微丝支架的可渗透引导通道增强轴突生长和成熟”。《生物材料研究杂志 A 部分》。75A(2):374-386。doi:10.1002/jbm.a.30432。PMID 16088902。
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - ↑ Wu,Y.(2006)。“自组装 IKVAV 肽纳米纤维促进 PC12 细胞粘附”。《华中科技大学学报(医学版)》。26(5):594-596。doi:10.1007/s11596-006-0530-7。PMID 17219978。
{{cite journal}}: Unknown parameter|coauthors=ignored (|author=suggested) (help) - ↑ Forraz,N.;Wright,K. E.;Jurga,M.;McGuckin,C. P.(2013)。“中枢神经系统修复的实验疗法:干细胞和组织工程”。《组织工程与再生医学杂志》7:523-536。doi:10.1002/term.552。
- ↑ William M Pardridge,脑部药物递送,《脑血流和代谢杂志》(1997)17,713-731
- ↑ Menei P,Montero-Menei C,Venier MC,Benoit JP,使用聚(乳酸-共-乙醇酸)微球将药物递送至大脑,《药物递送专家意见》(2005 年 3 月)2(2):363-76
- ↑ "''融合技术''"。Wtec.org. Retrieved 2012-05-18.
- ↑ 增强技术小组(1998)。“小组成员的著作”. Retrieved 2007-02-02.
{{cite journal}}: Cite journal requires|journal=(help) - ↑ a b Roco,Mihail C. 和 Bainbridge,William Sims,eds.(2004)。融合技术以提高人类绩效。施普林格。ISBN 1-4020-1254-3。
{{cite book}}:|author=has generic name (help)CS1 maint: multiple names: authors list (link) - ↑ Agar,Nicholas(2004)。自由优生学:为人类增强辩护。ISBN 1-4051-2390-7。
- ↑ Parens,Erik(2000)。增强人类特质:伦理和社会影响。乔治城大学出版社。ISBN 0-87840-780-4。
- ↑ Kringelbach ML,Jenkinson N,Owen SLF,Aziz TZ(2007)。“深部脑刺激的翻译原则”。《自然评论神经科学》。8:623-635。PMID 17637800。
- ↑ Ford, Alyssa (2005年5月至6月). "人类:混音". Utne 杂志. 检索于 2007-03-03.
- ↑ 莫尼,帕特·罗伊 (2002). "超越克隆:让健康的人'更好'". 检索于 2007-02-02.
{{cite journal}}: 引用期刊需要|journal=(帮助) - ↑ 福山,弗朗西斯 (2002). 我们后人类的未来:生物技术革命的后果. 法勒·斯特劳斯和吉鲁. ISBN 0-374-23643-7.
- ↑ 生物技术与人类未来研究所. "人类 '增强'". 检索于 2007-02-02.
{{cite journal}}: 引用期刊需要|journal=(帮助) - ↑ 迈克尔·豪斯凯勒,更好的人类?:理解增强项目,敏锐,2013,ISBN 978-1-84465-557-1.
- ↑ 更好,更好,最好:人类对增强的追求 邀请研讨会总结报告。由科学自由、责任和法律计划召开。美国科学促进会。2006 年 6 月 1 日至 2 日。作者:埃尼塔·A·威廉姆斯。编辑:马克·S·弗兰克尔。
- ↑ 休斯,詹姆斯 (2004). 公民赛博格:为什么民主社会必须应对未来的改造人类. 西景出版社. ISBN 0-8133-4198-1.
- ↑ 美国卫生与公众服务部.FDA 批准植入式脑刺激器来控制震颤。 检索于 2006 年 10 月 18 日。
- ↑ '脑起搏器' 治疗肌张力障碍。 KNBC 电视台,2003 年 4 月 22 日。检索于 2006 年 10 月 18 日。
- ↑ FDA 批准针对严重强迫症的深部脑刺激器的人道主义器械豁免。
- ↑ 美国国立神经疾病和中风研究所. 帕金森病深部脑刺激信息页面。 检索于 2006 年 11 月 23 日。
- ↑ Volkmann J, Herzog J, Kopper F, Deuschl G. "深部脑刺激器编程简介". 运动障碍. 2002 17, S181–187. PMID 11948775.
- ↑ Starr PA, Martin AJ, Ostrem JL, Talke P, Levesque N, Larson PS. 使用高场介入性磁共振成像和头骨安装瞄准装置的丘脑底核深部脑刺激器植入:技术和应用精度。神经外科杂志. 2010 年 3 月;112(3):479-90. doi: 10.3171/2009.6.JNS081161. PMID 19681683
- ↑ 深部脑刺激,匹兹堡大学神经外科系。检索于 2008 年 5 月 13 日。