有机化学/光谱学
有几种光谱技术可用于识别有机分子:红外 (IR)、质谱 (MS) 紫外可见光谱 (UV/Vis) 和核磁共振 (NMR)。
IR、NMR 和 UV/vis 光谱基于观察分子吸收和发射的电磁辐射的频率。MS 基于测量分子的质量以及在 MS 仪器中可能产生的任何分子碎片的质量。
紫外可见光谱是一种吸收光谱技术,它利用 10 纳米到 700 纳米范围内的电磁辐射。这些波长之间光的能量可以被驻留在分子轨道中的非键合 n 电子和 π 电子吸收。这种能量的吸收会导致电子从最高占据分子轨道 (HOMO) 跃迁到最低未占据分子轨道 (LUMO)。更具体地说,据说电子经历了 n→π* 跃迁或 π→π* 跃迁。正是这种可见光能量的吸收导致了色素化合物的感知颜色。由于这种现象,UV/Vis 是一种经常在有机化学中使用的技术,用于识别分子中是否存在自由电子或双键 (π) 键。分子最吸收的波长被称为 λ-max,正是这个数字可以用来对不同分子进行比较分析。这种光谱技术也可以使用 Woodward-Fieser 规则来识别一些具有大的共轭 π 系统或羰基的分子,该规则依赖于一组经验值来预测化合物的 λ-max。
核磁共振 (NMR) 波谱是确定有机化合物结构最有用的一种分析技术。NMR 主要有两种类型:1H-NMR(质子 NMR)和13C-NMR(碳 NMR)。NMR 基于原子核具有称为自旋的量子性质这一事实。当对 1H 或 13C 核施加磁场时,核可以与施加的磁场平行 (自旋 +1/2) 或反平行 (自旋 -1/2) 排列。
这两个状态具有不同的势能,能量差取决于磁场强度。然而,原子核周围磁场的强度取决于原子核周围的化学环境。例如,原子核周围和附近的负电荷电子可以屏蔽原子核免受磁场的影响,从而降低原子核感受到的有效磁场强度。这反过来将降低在 +1/2 和 -1/2 状态之间跃迁所需的能量。因此,连接到供电子基团(如烷基)的原子核的跃迁能量将更低,而连接到吸电子基团(如羟基)的原子核的跃迁能量将更高。
在 NMR 机器中,被分析的化合物被放置在一个强磁场中,并用无线电波照射,使所有 1H 和 13C 原子核都占据高能的 -1/2 状态。当原子核恢复到 +1/2 状态时,它们会释放出与两种自旋状态之间的能量差相对应的无线电波。无线电波被记录下来,并由计算机分析以给出样品的强度与频率图。然后,可以使用这些信息来确定化合物的结构。
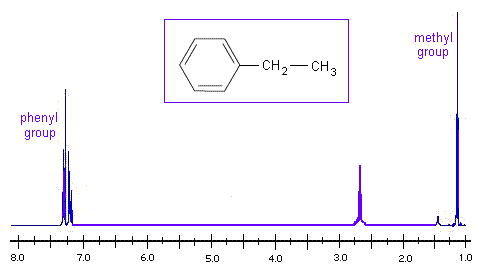
H-NMR 中的芳香族 供电子基团与吸电子基团
在单取代环上,供电子基团在较高的化学位移处共振。供电子基团通过将电子释放到反应中心来增加电子密度,从而稳定碳正离子。甲基 (-CH3) 是供电子基团的一个例子。
相应地,吸电子基团在较低的化学位移处表示。吸电子基团将电子从反应中心拉走。这可以稳定富电子碳负离子。卤素 (-Cl, -F) 和羧酸 (-COOH) 是吸电子基团的一些例子。
观察乙苯的 H NMR 谱,我们可以看到甲基是最强的吸电子基团,因此它出现在最低的化学位移处。芳香苯基是最强的供电子基团,因此它具有最高的化学位移。
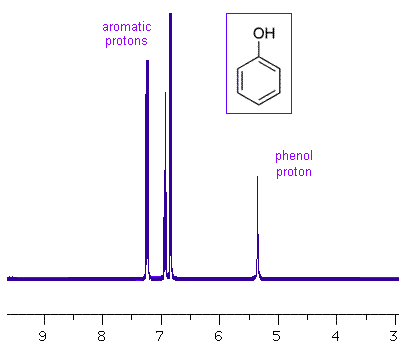
二取代环
整个芳香区域的积分强度值的总和显示了有多少取代基连接到环上,因此总值为 4 表明环具有 2 个取代基。当苯环具有两个取代基时,每个取代基都会对随后的取代反应产生影响。引入新取代基的位点取决于现有基团的取向及其各自的导向效应。对于二取代苯环,有三种可能的 NMR 模式。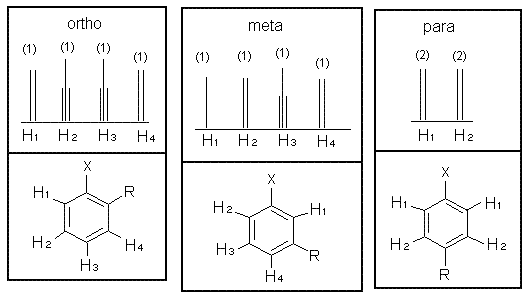
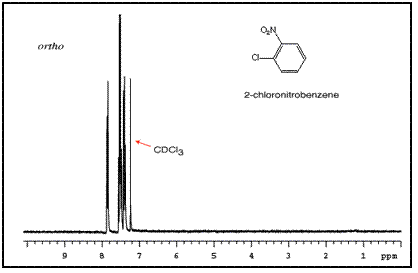
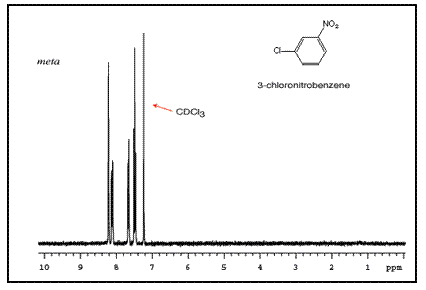
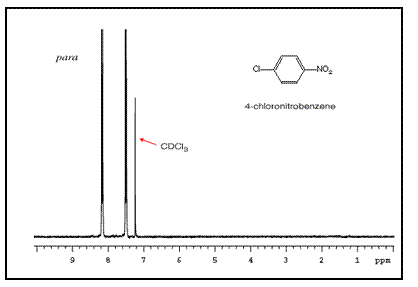
请注意,对位取代环通常显示两组对称的峰,看起来像双峰。
这些峰的顺序取决于两个取代基的性质。例如,氯硝基苯异构体的三个 NMR 谱如下
质谱仪测量离子相对于电荷的精确质量。很多时候,会事先进行某种形式的分离,从而能够在相对纯净的样品上收集光谱。可以将有机样品引入质谱仪并使其电离。这也将一些分子分解成更小的碎片。
所得的质谱显示
1) 最重的离子只是电离的分子本身。我们可以简单地记录它的质量。
2) 其他离子是分子的碎片,并提供有关其结构的信息。常见的碎片是
| 种类 | 公式 | 质量 |
| 甲基 | CH3+ | 15 |
| 乙基 | C2H5+ | 29 |
| 苯基 | C6H5+ | 77 |
吸收红外辐射使共价键振动。不同类型的键吸收不同波长的红外线
红外光谱学家不是记录波长,而是记录波数;在一厘米中能容纳的波数。(这很容易转换为波的能量。)
出于某种原因,光谱是反向记录的(从 4000 到 500 cm-1 是典型的),通常在 1000 cm-1 以下使用不同的刻度(以便更清楚地看到指纹区域),并且颠倒(记录的是 % 辐射透射率而不是辐射吸收率)。
吸收的 IR 辐射的波数是许多键的特征,因此 IR 光谱可以确定样品中包含哪些官能团。例如,羰基 (C=O) 键将在 1650-1760cm-1 处吸收。
| 键 | 最小波数 (cm-1) | 最大波数 (cm-1) | 官能团(以及其他注意事项) |
| C-O | 1000 | 1300 | 醇和酯 |
| N-H | 1580 | 1650 | 胺或酰胺 |
| C=C | 1610 | 1680 | 烯烃 |
| C=O | 1650 | 1760 | 醛、酮、酸、酯、酰胺 |
| O-H | 2500 | 3300 | 羧酸(非常宽的带) |
| C-H | 2850 | 3000 | 烷烃 |
| C-H | 3050 | 3150 | 烯烃(将强度与烷烃进行比较,以大致了解所涉及的 H 原子的相对数量。) |
| O-H | 3230 | 3550 | 醇中的氢键 |
| N-H | 3300 | 3500 | 胺或酰胺 |
| O-H | 3580 | 3670 | 醇中的游离 –OH(仅在用非极性溶剂稀释的样品中) |
列出的吸收以 cm-1 为单位。


产生一束红外光,并将其分成两束独立的光束。一束穿过样品,另一束穿过参考,参考通常是样品溶解的物质。这两束光都反射回探测器,但首先它们通过一个分离器,分离器快速交替使两束光中的哪一束进入探测器。然后比较两个信号,并获得打印输出。
使用参考有两个原因
- 这可以防止光源输出的波动影响数据
- 这使得可以抵消溶剂的影响(参考通常是样品所处溶剂的纯净形式)。
SDBS 是一个免费的在线光谱分析数据库,包含许多红外光谱、核磁共振光谱和质谱图。