气体中的粒子由于彼此之间的碰撞而随机地失去和获得能量。 平均而言,对于大量的粒子,具有至少一定能量 ε 的粒子的比例是恒定的。 这被称为玻尔兹曼因子。 它是一个介于 0 到 1 之间的值。 玻尔兹曼因子由以下公式给出
 ,
,
其中 n 是动能高于能量水平 ε 的粒子数量,n0 是气体中粒子的总数,T 是气体的温度(以开尔文为单位),k 是玻尔兹曼常数(1.38 x 10−23 JK−1)。
这种能量可以是粒子可能具有的任何类型的能量 - 例如,它可以是重力势能或动能。
在大气中,粒子受到重力向下拉。 由于彼此之间的碰撞,它们获得和失去重力势能 (mgh)。 首先,让我们考虑一小块大气。 它具有水平横截面积 A,高度 dh,分子密度(每单位体积的分子数)n,并且所有分子都具有质量 m。 令块中的粒子数为 N。

所以
 (如果你仔细想想,这是有道理的)
(如果你仔细想想,这是有道理的)
根据定义

总质量 Σ m 是单个分子的质量 (m) 乘以分子数量 (N)

然后计算块的重量

向下的压力 P 是每单位面积的力,因此

我们知道,当我们在大气中上升时,压力会下降。 因此,在我们的小块中,存在由以下公式给出的压力差 dP
 (1)换句话说,压力正在下降 (-),它是这一小块大气重量的结果。
(1)换句话说,压力正在下降 (-),它是这一小块大气重量的结果。
我们也知道

所以

但是

所以,通过替换

所以,对于我们的小块
 (2)
(2)
如果我们将 (1) 和 (2) 等同

重新排列以获得


在 n0 和 n 的极限之间积分
![{\displaystyle h={\frac {-kT}{mg}}\int _{n_{0}}^{n}{\frac {1}{n}}\;dn={\frac {-kT}{mg}}\left[\ln {n}\right]_{n_{0}}^{n}={\frac {-kT}{mg}}\left(\ln {n}-\ln {n_{0}}\right)={\frac {-kT}{mg}}\ln {\frac {n}{n_{0}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/56959ced2af27584ee8e2e47b7a9d9a4db5761b3)


由于我们正在处理重力势能,ε = mgh,所以

此主题在 2010 年 6 月 Q10 494 中出现。该问题中使用的各种值的数值为

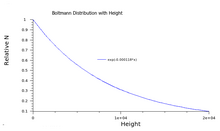 显示如何通过高度获得能量
显示如何通过高度获得能量
1u = 1.66 x 10−27 kg
g = 9.81 ms−2

1. 氮气分子的分子量为 28u。如果地球大气层是 100% 氮气,温度为 18 °C,那么有多少比例的氮气分子能达到 2 km 的高度?
2. 在 0 °C 下,一箱氢气(分子量为 2u)中,有多少比例的分子速度大于 5ms−1?
3. 如果一半的氢气以至少 10ms−1 的速度运动,那么氢气的温度是多少?
4. 一些电离的氢气(电荷 -1.6 x 10−19 C)放置在均匀的电场中。两极板之间的电位差为 20V,两极板之间的距离为 1m。在 350°K 的情况下,有多少比例的分子距离正极板至少 0.5m(忽略重力)?
解题步骤


















![{\displaystyle h={\frac {-kT}{mg}}\int _{n_{0}}^{n}{\frac {1}{n}}\;dn={\frac {-kT}{mg}}\left[\ln {n}\right]_{n_{0}}^{n}={\frac {-kT}{mg}}\left(\ln {n}-\ln {n_{0}}\right)={\frac {-kT}{mg}}\ln {\frac {n}{n_{0}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/56959ced2af27584ee8e2e47b7a9d9a4db5761b3)



