核医学/患者剂量学基础物理
本章概述了MIRD方法,该方法用于估算核医学中的剂量,并给出了对一小部分检查的典型患者剂量的调查结果。还提供了 X 射线 CT 调查结果,以便进行比较,并帮助您了解 PET/CT 和 SPECT/CT 的剂量学影响。
直接测量核医学程序对人体器官的吸收剂量很少可能。大多数估计依赖于蒙特卡罗模拟。为了计算剂量分布,必须追踪数十万个源自多个源器官的虚拟伽马射线穿过人体,因为它们通过康普顿散射和光电吸收与组织相互作用。还必须包括来自俄歇电子、内转换电子和β衰变的剂量贡献。模拟的这后一部分通常非常简单,因为可以认为这些辐射是在它们起源的器官中吸收的。
美国的医疗内部辐射剂量 (MIRD) 委员会提供大量数据,以帮助进行剂量估算。MIRD 计算方法允许估算从均匀分布在特定源器官中的放射性物质对重要器官的剂量。该方法可以分为两个部分
- 首先,对人体内放射性物质的生物分布做出一些假设或进行测量,同时考虑标记的放射性核素的生物学半衰期和物理半衰期。
- 任何特定源器官的累积活性,Ãs,通过对瞬时活性随时间的积分来计算。这些数据可能来自理论建模(例如隔室分析)或来自使用伽马相机测量感兴趣器官中计数率随时间的变化 - 请参见下图
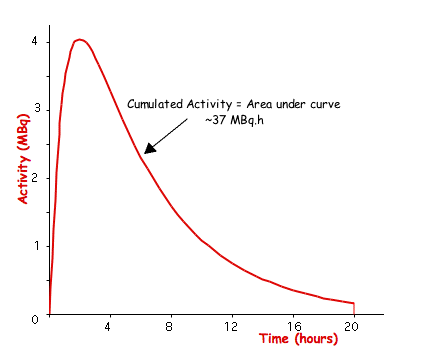
- 从数学上讲,这种活性/时间曲线可以用以下方程表示
- 其中 As(t) 是时间 t 时源器官 s 中的活性。
- 其次,目标器官 t 的吸收剂量 Dt 由以下公式计算
- 其中 s 上的求和旨在考虑所有源器官对目标器官的贡献。S 因子,S(t,s) 是从均匀分布在源器官 s 中的相应放射性核素的单位活性对目标器官 t 的平均吸收剂量。请注意,源器官和目标器官可能是同一个实体。
MIRD 方法中最具挑战性的部分是 S 因子的计算,因为它依赖于对放射性核素发射的辐射的准确了解。虽然 MIRD 出版物通过提供大多数器官和各种放射性核素的 S 因子的代表性值来提供帮助,但了解该方法以及因此该技术的局限性非常重要。
每种辐射类型的 S 因子可以分解为组成因子
其中
- D 是与特定辐射类型相关的总能量的度量,并且是来自放射性核素衰变方案的物理实体,
- f(t,s) 是源器官 s 中发射并在目标器官 t 中吸收的特定辐射的吸收分数,以及
- m 是目标器官的质量。
吸收分数表示特定类型辐射发射的总能量中在目标器官中吸收的比例。对于在组织中射程很短的β粒子,可以假设所有能量都将在源器官中沉积,而其他目标器官不会受到辐射。也就是说
除非 t = s,在这种情况下
在这种情况下,确定 S 因子非常简单。
然而,对于伽马射线,没有这种简单的方法,因为沉积在源器官和目标器官中的能量取决于
- 伽马射线能量以及
- 这两个器官的大小、形状和间距。
此外,我们不仅需要考虑来自放射性核素原子核的伽马射线,还需要考虑来自整个原子的发射,即当受到来自原子核的发射的刺激时,来自电子壳层的发射。以下表格以99mTc 为例说明了这种情况
| 辐射 | 辐射/衰变 | 辐射能量(keV) | 剂量(keV/衰变) |
|---|---|---|---|
| 来自 M 壳层的转换电子,γ1 | 0.75 | 1.63 | 1.21 |
| γ2 | 0.89 | 140.5 | 125 |
| 来自 K 壳层的转换电子,γ2 | 0.09 | 119.5 | 10.6 |
| 来自 L 壳层的转换电子,γ2 | 0.01 | 137.5 | 1.47 |
| 来自 M 壳层的转换电子,γ2 | 0.002 | 140.0 | 0.27 |
| 来自 N 壳层和外壳层的转换电子,γ2 | 0.0004 | 140.4 | 0.05 |
| K 层转换电子,γ3 | 0.006 | 121.6 | 0.67 |
| L 层转换电子,γ3 | 0.002 | 139.6 | 0.24 |
| M 层转换电子,γ3 | 0.0003 | 142.1 | 0.05 |
| Kα1 X 射线 | 0.04 | 18.4 | 0.74 |
| Kα2 X 射线 | 0.02 | 18.3 | 0.39 |
| Kβ X 射线 | 0.01 | 20.6 | 0.25 |
| K-俄歇电子 | 0.02 | 15.5 | 0.32 |
| L-俄歇电子 | 0.1 | 2.2 | 0.22 |
从表格中我们可以看到,原子整体会产生一系列辐射。例如,在第一行,原子核发射的伽马射线能量在约 75% 的一种类型同质异能跃迁中被传递到 M 层电子,使其具有 1.63 keV 的最大能量,即每个核衰变约 1.2 keV。在第二行,另一种同质异能跃迁产生的伽马射线在 89% 的情况下以 140.5 keV 的能量从原子中发出,或每个衰变约 125 keV。在第三种情况下,在约 9% 的这些后一种同质异能跃迁中,K 层中的电子获得 119.5 keV 的能量,这足以使其克服该层(约21 keV)的结合能并离开原子。请注意,荧光 X 射线(由于电子跃迁以填补 K 层的空位而产生)也会产生 - 以及俄歇电子。
下面复制了 99mTc 的 S 因子 MIRD 表的一部分,作为典型值的示例。
| 靶器官 | 肝脏作为源 | 脾脏作为源 |
|---|---|---|
| 膀胱壁 | 4.3 x 10-5 | 3.2 x 10-5 |
| 胃壁 | 5.1 x 10-4 | 2.7 x 10-3 |
| 肝脏 | 1.2 x 10-2 | 2.6 x 10-4 |
| 肺 | 1.4 x 10-4 | 6.2 x 10-4 |
| 胰腺 | 1.1 x 10-3 | 5.1 x 10-3 |
| 脾脏 | 2.5 x 10-4 | 8.9 x 10-2 |
S 因子的单位通常为 mGy/MBq/小时。请注意,实际值和计算值之间可能会出现重大差异,具体取决于个体患者在解剖结构和生理功能方面的差异。
肝脏扫描的剂量
[edit | edit source]为了说明上面的表格如何在假设情况下使用,假设对患者进行肝脏扫描,其中给患者注射 37 MBq 的 99mTc 标记的硫胶体。假设还发现从代谢模型中
- 80% 的累积活性进入患者的肝脏,并且
- 20% 进入他们的脾脏。
当假设胶体在这两个器官中的生物半衰期无限大时,这是一个合理的近似值,累积总活性的计算就大大简化了,如下面的方框所示。
需要注意的是,肝脏剂量几乎完全来自肝脏中的放射性物质,而脾脏中的放射性物质对肝脏剂量的贡献很小,仅占 5%。
类似地,脾脏的剂量可以计算为 5.8 mGy。请注意,虽然脾脏中积累的放射性物质较少,但吸收剂量却较高。然而,当您回想起吸收剂量是指单位质量吸收的能量时,就可以解决这个看似矛盾的情况。
国际放射防护委员会 (ICRP) 基于对被称为标准人的生理数据以及 MIRD 数据的了解,发表了更准确的器官吸收剂量。请注意,下表中肝脏和脾脏的吸收剂量分别为 2.74 和 2.85 mGy,略低于我们在上述简单假设情况下计算的结果。
| 靶器官 | wT | 吸收剂量 (mGy) | wT.HT (mSv) |
|---|---|---|---|
| 性腺 (F) | 0.2 | 0.081 | 0.016 |
| 红骨髓 | 0.12 | 0.41 | 0.049 |
| 结肠 | 0.12 | 0.07 | 0.008 |
| 肺 | 0.12 | 0.2 | 0.024 |
| 胃 | 0.12 | 0.23 | 0.028 |
| 膀胱 | 0.05 | 0.04 | 0.002 |
| 乳房 | 0.05 | 0.1 | 0.005 |
| 肝脏 | 0.05 | 2.74 | 0.137 |
| 食道 | 0.05 | 0.1 | 0.005 |
| 甲状腺 | 0.05 | 0.03 | 0.0015 |
| 骨表面 | 0.01 | 0.24 | 0.0024 |
| 脾脏 | 0.025 | 2.85 | 0.071 |
| 其余 | 0.05 | 0.21 | 0.005 |
请注意,通过对表格右栏中的值进行求和,可以得到 0.35 mSv 的有效剂量。
最后,请注意,在上述讨论中,为了简便起见,所有来自 99mTc 衰变的辐射能量都假设辐射加权因子 wR 为 1。
典型的核医学剂量
[edit | edit source]下表列出了几种核医学程序的有效剂量(改编自 ICRP 53)
| 检查 | 放射性药物 | 活性 (MBq) | 器官 | 吸收剂量 (mGy) | 有效剂量 (mSv) |
|---|---|---|---|---|---|
| 骨扫描 | 99mTc-MDP | 740 | 骨 膀胱 |
46 38 |
4.2 |
| 心壁 | 201Tl-氯化铊 | 120 | 睾丸 结肠 肾脏 |
68 44 65 |
26(M) 16(F) |
| 感染 | 67Ga-柠檬酸镓 | 150 | 骨 结肠 红骨髓 肾上腺 脾脏 |
94 25 31 14 15 |
15 |
| 肾图 | 99mTc-DTPA | 150 | 膀胱 | 9.3 | 0.73 |
| 肝脏扫描 | 99mTc-硫化胶体 | 74 | 肝脏 脾脏 |
5.2 5.6 |
0.7 |
| 肺灌注 | 99mTc-MAA | 74 | 肺 肝脏 |
4.9 1.2 |
0.8 |
| 肺通气 | 99mTc-锝气 | 20 | 肺 | 2.2 | 0.3 |
| 甲状腺扫描 | 99mTc-高锝酸盐 | 185 | 结肠 胃 甲状腺 |
8.0 4.8 4.1 |
1.9 |
| 甲状腺扫描 | 131I-碘化钠 | 150 | 膀胱 胃 |
91 5 |
9.2 |
| PET 扫描 | 18F-2-脱氧葡萄糖 | 180 | 膀胱 心脏 |
29 11 |
3.4 |
请注意,99mTc 扫描的典型有效剂量大约为几 mSv。另外请注意,201Tl 扫描的有效剂量很高,部分原因是睾丸中积累的放射性物质很多,以及 67Ga 和 131I 的有效剂量也很高。表格中列出的给药活性与 2000 年对澳大利亚和新西兰核医学实践调查中发现的最常用活性一致。
X 射线 CT 的典型剂量
[edit | edit source]X 射线 CT 对患者的辐射剂量由许多因素决定,包括辐射能量和强度特性、患者大小、辐射探测器的效率,以及图像采集所用特定形式的因素(例如,轴向扫描与螺旋扫描)。
患者体内的吸收剂量并不均匀,皮肤上的剂量最高,被照射区域中心约低三倍。皮肤吸收剂量的典型值范围约为 5 mGy 到 50 mGy。头部扫描的吸收剂量通常高于身体扫描的吸收剂量,因为颅骨的衰减很大。此外,眼球晶状体可以接受相对较大的剂量,通常为 50 到 100 mGy,如果重复检查,可能会超过白内障诱导的确定性限值。应制定使用适当的机架角度的方案,以最大限度地减少眼球直接照射的可能性。同样,腹部或骨盆 CT 扫描会导致相对较大的子宫剂量,这在扫描育龄妇女时可能是一个问题。
近年来已经发表了一些调查,估计了 CT 扫描的有效剂量,见下表。数据表明,有效剂量通常为 2 到 20 mSv,较高值与腹部和骨盆 CT 扫描相关,而较低值与头部和颈椎扫描相关。这种差异很大程度上反映了可能被初级射线照射的放射敏感器官的数量。不同国家之间的剂量差异则是一个不同的问题!
| 检查 | 新西兰 | 澳大利亚 | 英国 |
|---|---|---|---|
| 头部 | 2.2 | 2.7 | 1.8 |
| 胸部 | 9.8 | 10.7 | 7.8 |
| 腹部 | 11.6 | 17.5 | 7.6 |
| 肝脏 | 6.5 | 13.4 | 7.2 |
| 腰椎 | 5.0 | 5.4 | 3.3 |
| 骨盆 | 7.2 | 11.2 | 7.1 |
请注意,核医学程序的有效剂量与 CT 检查的有效剂量处于同一数量级,但通常更低。为了帮助您进行比较:胸部 X 射线 的有效剂量约为 0.02 mSv,而 乳腺 X 线检查 的有效剂量约为 0.4 mSv,静脉肾盂造影 (IVP) 的有效剂量约为 3 mSv。这个数字与肾图的剂量相比如何?您不妨思考一下造成巨大差异的原因,作为进一步加深对该主题理解的练习。

















