核医学基础物理/三维可视化技术
这是一本名为核医学基础物理的华夏公益教科书正在编写的章节。
三维可视化技术用于将一系列断层扫描切片整合到一种形式中,这种形式通常比单独的切片更容易解释。本章介绍了医学成像中使用的主要可视化技术概述。我们将从二维 (2D) 轴向图像的整合开始,然后再考虑各种三维 (3D) 图像呈现方法。
以下图像集将用于帮助我们完成任务。它们包含一个 SPECT 肺通气研究(由左侧的动画序列说明)、一个 SPECT 肺灌注研究(在中间)和来自同一患者的 CT 肺血管造影术(CTPA)(在右侧)。
 |
 |
 |
我们将在这章的各个阶段使用这些图像集,以便提供有助于演示我们将要考虑的技术本质的示例。图像集的采集因素包括 SPECT 研究的每个 128 x 128 像素切片厚度为 4.8 毫米,CTPA 螺旋扫描重建的轴向图像的每个 512 x 512 像素连续切片厚度为 1.5 毫米。此外,肺灌注扫描是在通气扫描之后立即进行的,因此来自前者的残余活性以约 20% 的水平存在于后者中。
在继续之前,考虑一下轴向切片(无论是 SPECT 还是 CT),一个接一个地堆叠在一起,如下图所示。

请注意,该图将每个图像表示为一个薄切片,而数据实际上代表一个足够宽的切片,可以填补它与其下一个切片之间的间隙,因此可以认为图像数据是体积元素矩阵,简称体素。
医学成像中应用的一种惯例是,将轴向图像堆栈显示为以下图中所示的轴向。

因此,轴向扫描的左侧代表患者的右侧,从下方观看,其前表面位于图像的顶部。斯派克·米利根的一首小曲的改编版可能会帮助你记住这种视角。
| 我多么想成为一条鱼, |
| 能在冰层下游泳, |
| 向上看所有滑冰的人, |
| 哦,那该多好! |
你可能会发现,在阅读本章时体验真实情况是一个好主意,这样有助于克服我们将遇到的许多主题的抽象性,以及使用二维媒介(即本网页)传达三维可视化概念的局限性。无数开源 3D 程序和图像库可通过万维网获取。例如,用于生成本章图像的软件包括OsiriX(仅适用于 macOS X)、Madena和ImageJ(多平台)。
我们将要考虑的第一个技术是一个相对简单的技术,称为轴向投影。它涉及整合多个轴向图像以显示一个复合图像,该复合图像呈现该体积图像数据的三维印象。该技术有时被称为厚板或Z 投影。
下图说明了一系列 z 投影方法的结果,右下角显示了一个单切片以供参考。左上角的第一张图像显示了对 16 个切片求和的结果,同一行上的另外两张图像分别显示了计算这些切片的平均值和中位数的结果。

第二行中的前两张图像分别显示了最大强度投影(MIP)和最小强度投影(MinIP)的结果。MIP 会评估穿过体积的每条体素线上的每个体素,以确定最大体素值,并使用为每条线确定的这些值形成图像。MinIP 使用最小体素值,如下面的图所示。

底部一行示例轴向投影集合中的前两张图像显示了体绘制投影。这种图像合成方法涉及对体素数据应用不透明度函数以及对所得数据的递归添加。以下形式的方程
其中
- An = (α).(体素 n 的体素值),
- Bn = (1-α).(体素 n-1 的体素值),并且
- α = 不透明度,范围在0(即完全透明)到1(即完全不透明)之间,
应用于每条体素线,如下图所示。

该图显示了我们之前使用过的体素线,右上角有一个不透明度表。显示的不透明度函数是其中对低于阈值级别的体素值应用零不透明度、对中间范围的体素值应用不透明度的线性增加、以及对高体素值应用最大不透明度的函数。不透明度表有点像我们之前描述过的用于灰度窗口的查找表早先,该函数应用于体素值的不透明度而不是它们的灰度级别。请注意,也可以应用比我们在上面的图中使用的更复杂的不透明度表,例如对数函数和指数函数。
图的下半部分显示了计算复合体素的体绘制值的步骤。体素值显示在第一行,不透明度值显示在第二行,这些不透明度值来自一个粗略的不透明度表,用于显示每个体素。第三、第四和第五行详细说明了A、B和C的值,这些值是使用我们上面的体绘制方程计算得出的。最终的体素值是通过对最后一行求和得到的,并将结果归一化为,比如说,256 级灰度。
这种处理形式的结果是生成一个图像,该图像包括视觉深度线索,因为类似的体素值将以类似的不透明度显示,而最靠近参考切片的体素将比来自更远切片的体素具有更强的贡献。此外,请注意,每条线中的所有体素值都会对渲染的图像做出贡献,这与仅对 MIP 或 MinIP 图像做出贡献的有限数量的体素形成对比。体绘制会产生 3D 效果,如上面的图像所示。
请注意,体绘制可以从远端到近端切片应用,如我们的图所示,也可以从相反方向应用,即从近端到远端切片。因此,我们在上面的一组九个示例图像中使用了体绘制向上和体绘制向下这两个术语。
选择适合个体患者研究的轴向投影方法类型取决于诊断过程中相关的解剖和/或功能信息。例如,让我们以对我们上面九个示例图像中对比剂填充的血管成像为例。请注意,MIP 可用于直观地展现患者肺部血管床的印象。但是,这种投影中几乎没有深度信息,因此重叠和底层的血管可能会遮挡目标血管中可能存在的病变。因此,这种轴向投影形式在血管造影中的应用仅限于血管重叠不是问题的研究。在体绘制图像中包含体素透明度和深度加权解决了 MIP 处理的这一局限性。
最后需要注意的是,这种图像投影形式也可以应用于轴向切片的多分层重建,我们将在下一节中探讨......
多分层重建
[edit | edit source]在最简单的情况下,多分层重建 (MPR) 涉及生成与轴向切片堆叠成直角的透视图,以便生成冠状面和矢状面图像。我们将从描述这些正交投影开始本节,然后考虑它们同步的复合显示。我们还将描述该主题的三个变体:斜面重建、曲线重建和集成三维展示。
- 冠状面重建
- 在这里,图像堆叠被旋转,使 z 轴成为垂直轴,并使用平行排列的体素平面重建图像堆叠,这些平面从患者的前表面到后表面排列,如下图所示

- 以下是我们图像集中示例冠状面重建的结果
 |
 |
- 在这里,重建的切片通常从患者的前表面到后表面显示,患者的头部朝向切片的顶部,右手侧朝向切片的左侧。
- 矢状面重建
- 通过对图像堆叠进行额外的旋转可以实现矢状面重建,从而生成患者从左到右的切片序列,如下图所示

- 以下是我们图像集中示例矢状面重建的结果
 |
 |
- 在这里,重建的切片通常从患者的左侧显示到右侧,头部朝向顶部,前表面朝向切片的左侧。请注意,也可以使用数据的额外几何变换生成从右到左的矢状面堆叠。
- 复合 MPR 显示
- 冠状面和矢状面重建被称为正交 MPR,因为生成的透视图来自相互成直角的图像数据平面。可以生成复合 MPR 显示,以便使用链接的游标或十字线从所有三个透视图定位感兴趣的点,如下图所示
 |
 |
- 这种图像展示形式有时被称为TCS 显示——意味着查看Transaxial、Coronal 和 Sagittal 切片。它可以与我们之前讨论的切片投影方法相结合,如下图所示的两个图像集,其中蓝线突出显示了冠状面投影的限制

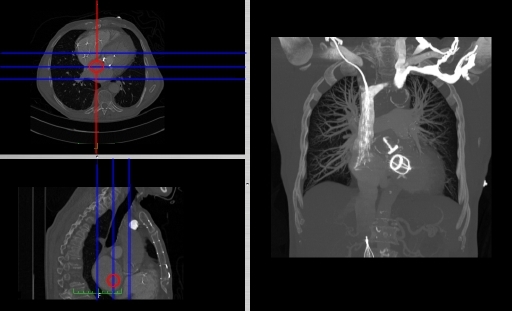
- 斜面重建
- 通过在体素数据中定义倾斜平面可以实现斜面 MPR,如下图所示

- 在这里,平面可以在轴向图像(左上角的红线)中定义,并且可以为重建的平面(右侧)显示最大强度投影(使用的限制由蓝线突出显示),例如。当试图生成透视图时,这种技术很有用,在这种情况下,三维结构的可视化因重叠的解剖细节而变得复杂。
- 曲线重建
- 曲线 MPR 可用于重建更复杂的透视图,如下图所示

- 在这里,可以在轴向图像(左面板)中定位一条曲线(以绿色突出显示),以定义一条延伸到 z 方向的体素数据的弯曲曲面,并且可以将来自该数据的体素重建成二维图像(右面板)。请注意,可以生成比图中所示更复杂的曲线,例如,可以隔离主要血管的三维走向,或者可以将 CT 头部扫描平面化以进行正畸应用.
- 3D 多平面重建
- MPR 主题的最后一个变体是生成一个三维显示,显示所有三个正交投影的组合,以便定义的感兴趣点定位平面的交点,如下图所示

- 为了说明目的,交点位于上述图形中体素数据的中心。它通常可以使用交互式控件放置在 3D 数据中的任何点。此外,通常可以交互地操纵用于旋转序列的透视图,以改善对感兴趣区域的可视化。请注意,上面图示的图像序列是可以通过这种方式生成的大量透视图中的一种。还要注意,切片投影(例如 MIP)可以与这种形式的显示相结合,以提供对感兴趣特征的额外透视图。
最大强度投影
[edit | edit source]我们在轴向投影的背景下描述了最大强度投影 (MIP),其中最大体素值是通过投影切片厚度平行运行的直线确定的。当这种计算应用于围绕体素数据进行连续角度的投影时,可以生成一系列这样的图像。一个简单的序列是围绕水平平面旋转 360 度,如下图左侧面板所示,其中最大强度投影到患者周围每 9 度,并将产生的 40 个图像编译成一个重复的时序(例如 电影)序列

请注意,3D MIP 从 CT 扫描的衰减最强的区域获取其信息(因为CT 数值直接取决于线性衰减系数),因此描绘了骨骼、对比介质和金属,而周围的衰减较低的组织几乎没有信息。还要注意,持续观看旋转 MIP 序列会产生令人不安的效果,其中旋转方向似乎周期性地反转——这可能是感知振荡的一个方面。上述图形中右侧面板中图示的透视 MIP 可以通过提供可用于指导持续视觉检查的空间线索来减少这种局限性。
透视投影可以通过从用于生成平行投影的平行线更改为体素线来生成,这些体素线从体积后面某个明显点发散,距离使得显示器的观看者可以将图像数据的更近特征可视化为相对大于更深特征——参见下图

体绘制
[edit | edit source]体绘制可以应用于体素数据,采用上面针对 MIP 描述的连续旋转方式,如下图所示的结果

请注意,可以增强体绘制的对比度,例如,通过体素值进行阈值化,以消除低衰减表面,如下图所示

还要注意,可以改变颜色查找表 (CLUT) 以突出显示特别感兴趣的特征,如下面的图像集所示

以下示例图像说明了不透明度表的影響
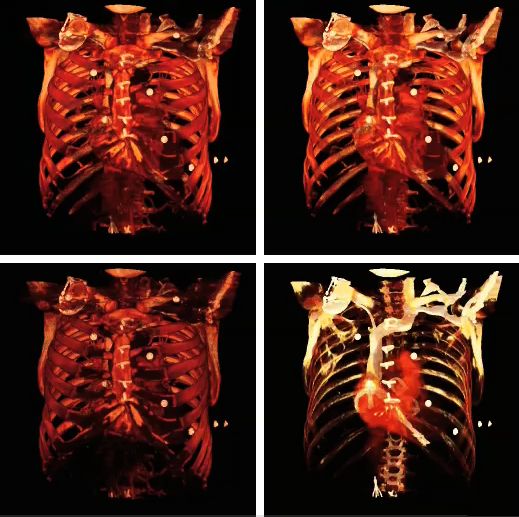
以下显示了各种阴影设置对体绘制的影响
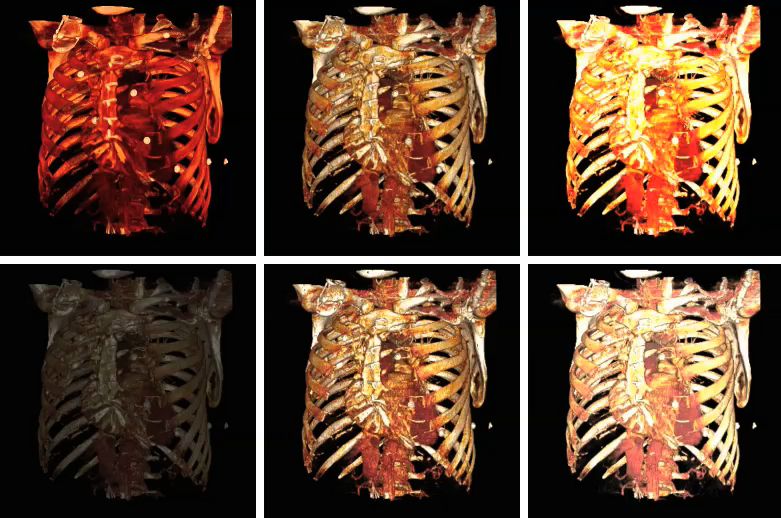
上面图像使用的阴影设置如下
| 图像 | 环境系数 | 漫射系数 | 镜面反射系数 | 镜面反射功率 |
|---|---|---|---|---|
| 左上角 | 0.15
|
0.9
|
0.3
|
15.0
|
| 中间顶部 | 0.75
|
0.9
|
0.3
|
15.0
|
| 右上角 | 0.15
|
0.1
|
0.3
|
15.0
|
| 左下角 | 0.15
|
0.9
|
1.2
|
15.0
|
| 中间底部 | 0.15
|
0.9
|
0.1
|
1.0
|
| 右下角 | 0.15
|
0.9
|
0.6
|
1.0
|
关于体绘制要说明的最后一个特征是,可以应用 3D 编辑技术,以从计算中排除不需要的特征并暴露内部结构。这在以下图形中有所说明,其中正交框架的平面可以移动以从六个方向裁剪体素数据。

表面渲染也称为阴影表面显示 (SSD),它涉及从 3D 数据中具有相似体素值的区域生成表面,如下面的左侧面板中显示的 SPECT 肺灌注扫描所示。

该过程涉及基于以下事实显示可能存在于 3D 体素数据中的表面:物体的边缘可以预期具有相似的体素值。一种方法是使用灰度阈值技术,其中一旦在投影线上遇到阈值,就会提取体素——请参见以下图表。然后使用三角形对提取的体素进行镶嵌,如上图右侧面板所示——并且使用恒定值填充三角形,并在模拟固定虚拟光源的效果的基础上应用阴影——如上图左侧面板所示。

可以将不透明度表应用于结果,以便还可以可视化内部特征的表面。例如,在下图中从 CT 扫描中识别出两个表面,其中来自骨表面的体素值以不透明的黄色编码,组织表面以透明的红色阴影编码。

在下图中显示了使用不透明度表的第二个示例。在这里,使用区域增长技术对来自患者气道轴向 CT 数据进行分割,然后使用表面渲染对结果进行处理,完全不透明,如左侧面板所示,并使用降低的不透明度 (30%),如右侧面板所示。

注意,当降低不透明度时,可以辨别每只肺的内部特征。还要注意,继续查看这种类型的透明度显示会产生图像旋转的明显反转,类似于上面提到的 3D MIP。克服此类问题的一种方法是例如分割每只肺并混合结果,如以下图所示。

我们将通过考虑 3D 可视化的一个应用来结束本章,该应用整合了我们在本华夏公益教科书中描述的许多图像处理技术。我们将在尝试可视化肺栓塞 (PE) 的特征性失配时,使用来自患者肺通气 (V) 和肺灌注 (Q) 研究的两个 SPECT 扫描。我们将考虑的应用程序称为subFusion 处理,因为它涉及图像减法和图像融合技术。
再次注意,SPECT 研究是使用淹没技术生成的,其中灌注扫描在使用产生扫描之间约 5:1 的相对计数率的给药活性后立即获取通气扫描。因此,第一个图像处理步骤是校正灌注扫描的背景通气活性。
由于在这种情况下通气示踪剂是使用气雾剂给药的,我们可以简单地假设它的生物分布在这两个扫描中是相当相同的。此外,由于扫描是在使用99mTc 放射性同位素相隔约 15 分钟后获取的,我们可以假设放射性衰变的影响可以忽略不计。因此,基于这些假设,我们可以简单地从灌注堆栈中减去通气堆栈,以隔离我们将称为“纯灌注”扫描的内容。
第二步是通过将通气堆栈乘以一个因子来归一化两个扫描,使得两个堆栈中的平均计数(例如)相似。
- 现在我们可以比较苹果和苹果了!
由于 PE 失配很可能来自肺部的区域,这些区域在通气扫描中包含计数,而在灌注扫描中相对缺乏此类计数,因此我们可以将“纯灌注”堆栈从通气堆栈中减去,作为第三个图像处理步骤,以隔离任何此类差异作为正值特征。
最终的图像处理步骤是将此差异堆栈与“纯灌注”扫描一起进行体积渲染,并将结果混合,如以下图像所示。

以下图示出了所涉及的步骤。请注意,为了简单起见,图中省略了一些次要过程,例如 CLUT 选择、相对不透明度调整和对比度增强。还要注意,在患者在两次 SPECT 获取之间发生移动的情况下,可能需要在程序开始时包含图像配准步骤。

最后一点需要注意的是,与 SPECT 图像相比,分割的 CTPA 图像中患者肺的尺寸更大。这是因为 CTPA 研究是在单次屏气下获取的,而 SPECT 研究是在患者在伽马相机旋转期间安静呼吸的情况下获取的。因此,三组图像的配准无法直接进行,需要应用空间扭曲和其他技术,不幸的是,这些技术超出了我们这里处理的范围。
