结构生物化学/脂类/膜转运
所有细胞都需要从周围的细胞外液中获取所需的分子和离子。在细胞壁内外以及在膜结合的细胞内区室(如细胞核、内质网和线粒体)之间存在着分子和离子的交换。通过膜交换的物质包括葡萄糖、Na2+ 和 Ca2+、ATP、mRNA 等。细胞膜的脂质双层对大分子和极性分子不透,但对水分子和其他小不带电分子(如 O2 和 CO2)可透。为了解决这个问题,细胞膜包含对独特的、水溶性分子有选择性的蛋白质。连续的蛋白质通路由载体蛋白、通道和泵组成。转运可以是载体蛋白利用能量源的主动转运,也可以是通过通道的协助扩散或被动转运。细胞的活动取决于它可以完成的生化反应,而这些反应又取决于从细胞外液中提取的化合物。任何给定细胞中表达的转运蛋白阵列定义了细胞的功能和效率。
任何分子或离子沿浓度梯度或逆浓度梯度运动的过程或运动都需要自由能变化。理解自由能是理解分子如何在浓度梯度中转运和/或行为的关键。根据热力学第二定律,分子会自发地从高浓度区域移动到低浓度区域。自由能的可用性是决定分子是否会穿过膜的因素之一,另一个因素是分子在脂质双层中的渗透性。将无电荷物质从浓度为 x1 的膜的一侧转运到浓度为 x2 的膜的另一侧的自由能变化如下所示:
ΔG (x) = RT ln (x2/x1) = 2.303 RT log10 (x2/x1)
R: 气体常数,8.314 x 10−3 kJ mol−1 K−1
T: 温度
x: 浓度
ΔG: 自由能
在 25° (298K) 时,ΔG 为 +11.4 kJ mol−1 (+2.7 kcal mol−1),表明此转运过程需要能量输入。
对于带电物质,由于“同类”电荷会相互排斥,因此跨膜的离子电荷不均匀分布会导致产生电势。将电项和浓度相加,电势生成一般表达式。
ΔG (x) = RT ln (x1/x2) + Ζ F ΔV = 2.303RT log10 (x2/x1) + Ζ F ΔV
Ζ: 转运物质的电荷。
F: 法拉第常数 96.5 kJ V−1 mol−1。
ΔV: 跨膜的电势(伏特)。
当 ΔG 为正值时,转运是主动的,需要能量输入才能将分子逆浓度梯度移动,与 ΔG 为负值相反,转运是被动的,这意味着这些分子会沿其自身的梯度穿过膜,即简单扩散。

被动转运是在不使用化学能的情况下将生化物质跨越细胞膜的过程。四种主要类型包括扩散、协助扩散、过滤和渗透。
扩散是指分子从高浓度区域迁移到低浓度区域,穿过细胞膜的过程。当分子数量稳定时,这种状态称为平衡。这是通过随机分子运动发生的。
扩散系数是一个比例因子,它代表了物质在单位时间内通过单位浓度梯度跨单位面积的扩散量。它用 D 表示,基于菲克扩散定律。
有两种扩散:
1) 示踪扩散是在没有浓度梯度的情况下发生的分子自发混合。这种扩散在平衡状态下进行。
2) 化学扩散在存在浓度梯度的情况下发生。它将导致净质量转运。整个系统的熵将增加,它将逐渐接近平衡,直到达到平衡。
其他类型的扩散包括:
- 渗透是指水通过半透膜的扩散。水将从水浓度较高的区域移动到水浓度较低的膜另一侧。渗透在生物系统中非常重要,因为许多膜是半透的。它们对有机溶质(即大分子)不透,但对水和小不带电溶质可透。渗透性不仅取决于大小,还取决于溶解度特性、电荷和化学性质。更多信息:[1]
- 原子扩散是一种扩散过程,它包含固体中原子随机热激活运动,最终导致原子的净转运。例如,气球内的氦原子如何通过气球壁扩散。气球最终会瘪掉。
- 布朗运动是指悬浮在流体(可能是液体或气体)中的粒子的随机运动。还存在一个数学模型来描述这种随机运动。
- 集体扩散是指大量粒子的扩散。这通常发生在溶剂内。这与布朗运动不同,因为布朗运动是单个粒子的扩散,并且可能需要考虑粒子之间的相互作用。
- 涡流扩散也称为“湍流扩散”。它是任何扩散过程,通过该过程,物质由于涡流运动而在大气或任何流体系统中混合。
- 逸散是指单个分子在没有分子之间碰撞的情况下流过孔的过程。如果孔的直径明显小于分子的平均自由程,就会发生这种情况。
离子通道是形成穿过膜的水填充孔的蛋白质,这些孔允许特定离子被动地沿电化学梯度转运。例如,人体中常见的离子通道包括 Na+ 通道、K+ 通道、Ca2+ 通道和 Cl- 通道。这些被动转运离子通道利用电化学势来驱动生理过程,例如神经冲动。电化学势由各种主动转运机制维持,例如 Na+-K+ ATP 酶。
离子通道的选择性源于形成蛋白质的氨基酸。决定哪些离子能够无阻碍地通过这些通道的两个主要标准是:孔隙的直径和氨基酸的电学性质。离子通道本质上是在膜的脂质双层中形成一个洞。洞的直径有助于决定哪些物质被允许通过通道。只有大小合适的离子才能通过特定离子通道的洞。一些较大的离子通道只允许特定离子通过而较小的离子不能通过,这一现象基于离子通过时脱水的能量学。通道内氨基酸羰基的排列决定了通道:羰基的排列使得某些水合离子的脱水能量成本最低。因此,较大的孔对较大的水合离子有有利的排列,而较小的水合离子通过则需要更多的能量来脱水。在钾通道中,这种介导 K+ 离子通过的脱水区域被称为选择性过滤器。
除了孔的直径外,氨基酸的电学性质也有助于决定哪些离子被允许通过离子通道。如果面向孔隙内部的氨基酸带负电荷,那么只有阳离子才能通过通道。阴离子由于静电排斥而会被通道中带负电荷的氨基酸排斥。反之,阴离子将能够通过带正电荷的氨基酸排列的通道。
有一些遗传性的离子通道疾病。其中包括:- 氯离子通道疾病包括囊性纤维化和遗传性肾结石倾向。- 钾离子通道疾病包括一些遗传性的危及生命的的心脏缺陷,新生儿罕见的遗传性癫痫倾向以及几种类型的遗传性耳聋。- 钠离子通道疾病包括遗传性的某些类型的肌肉痉挛倾向和利德尔综合征。
孔蛋白
[edit | edit source]
孔蛋白是一种膜蛋白,它在脂质双层中形成一个β桶孔。与其他蛋白质转运通道不同,孔蛋白的孔隙足够大,允许被动扩散。由于孔径较大,孔蛋白通常介导小代谢物如氨基酸、糖和离子的扩散。
各种孔蛋白的总体结构特性相同,无论它们的类型如何。孔蛋白是主要由β折叠组成的蛋白质,以反平行方向连接。十六到十八条β折叠链折叠成一个圆柱形管,称为β桶。氨基酸序列大致是非极性和极性残基交替排列,它们以适当的方式排列,以产生三级桶结构。这个β桶位于脂质双层中,形成进入细胞的大洞。由于这些相互作用,面向β桶外部的氨基酸通常是非极性的,与脂质双层的非极性区域相互作用。然而,β桶的内部通常包含极性氨基酸,以与连接膜两侧的水性环境相互作用。
孔蛋白也存在于革兰氏阴性菌的外膜中。革兰氏阴性菌含有外膜,有助于阻止不必要的化学物质进入,并增加毒力。孔蛋白促进小分子和营养物质通过外膜扩散进入周质空间。
离子载体
[edit | edit source]离子载体是帮助将离子从亲水性环境转运到疏水性环境的分子。换句话说,离子载体是帮助转运亲水性离子跨越脂质双层膜的离子载体。离子载体跨越细胞膜转运离子的两种主要机制是:载体和通道形成。
在载体机制中,离子载体与离子形成复合物。离子载体用其极性内部包裹离子。离子载体-离子复合物的外部主要是疏水性的,因此允许复合物穿过疏水性的细胞膜。载体离子载体基本上通过溶剂化屏蔽离子在环境中的电荷。
对于通道形成机制,离子载体通过脂质双层膜诱导一个亲水性通道。这个极性孔的形成允许离子穿过细胞膜。离子载体可以作为抗生素使用,因为它能够破坏跨膜电化学梯度。这种电化学梯度对于驱动代谢过程至关重要。如果没有梯度,就不会有离子进出细胞的净运动,本质上会破坏正常的细胞过程。离子载体通过允许离子自由扩散穿过细胞膜(形成复合物或通道)来破坏电化学梯度。这种自由扩散破坏了细胞质和细胞外环境之间的正常离子平衡,从而消除了电化学梯度。
协助扩散
[edit | edit source]协助扩散几乎发生在所有细胞中。离子的协助扩散是通过嵌入质膜中的蛋白质或蛋白质组合进行的。这些蛋白质是水填充的通道,离子可以通过这些通道沿浓度梯度移动。这些通道可以打开或关闭,而其他通道可以被认为是“门控”的。
一个重要的例子是葡萄糖的代谢。葡萄糖分子不能轻易通过细胞膜;单纯的被动扩散速度很慢,这对细胞代谢来说可能是一个问题。自然界解决这个问题的方法之一是协助扩散(另一种快速的葡萄糖转运方式是主动扩散)。与被动扩散一样,葡萄糖的移动始终是从葡萄糖浓度高的区域到低的区域,并且独立于离子偶联。葡萄糖转运蛋白催化葡萄糖跨膜移动的反应。葡萄糖分子的协助扩散速度快,双向进行。葡萄糖转运蛋白的作用类似于酶介导的催化。 [2]
协助扩散是一种被动转运形式,它不需要能量来转运分子和物质穿过细胞膜。它在很大程度上借助于膜的组成部分蛋白。协助扩散是指物质或分子穿过膜穿过特定的跨膜转运蛋白的自发通过。亲水性物质可以通过转运蛋白,避免与膜的脂质双层核心接触。一些这些蛋白质的功能是通过一个亲水性通道来实现的,该通道可以让极性分子通过。水通道蛋白是通道蛋白的例子,它促进水分子通过膜的转运。其他称为载体蛋白的蛋白质会抓住分子并改变形状,从而避免分子与疏水性核心接触,并穿过膜。大多数蛋白质具有很高的特异性,即它们只转运特定类型的物质。
门控离子通道
[edit | edit source]配体门控
这些离子通道在与信号分子或“配体”结合时打开或关闭。配体不是通道打开时转运的物质。一些离子受细胞外配体门控,另一些受细胞内配体门控。
另一种类型的蛋白质通道是让离子通过的离子通道。其中许多受电信号或化学信号刺激,被称为门控通道。刺激物要么打开通道,要么关闭它们。例如,神经细胞受某些神经递质分子刺激,会打开门控通道,允许钠离子进入细胞。外部配体与通道细胞外侧的位点结合。示例包括
- 乙酰胆碱(Ach),它是在某些突触处神经递质乙酰胆碱的结合。它打开允许钠离子进入的通道,并启动神经冲动或肌肉收缩。
- γ-氨基丁酸(GABA) - GABA 在某些突触处的结合允许中枢神经系统允许氯离子进入细胞,这抑制了神经冲动的产生。
- 钙通道,允许钙离子流入膜中。然后,这些 Ca2+ 离子充当第二信使内部配体,启动各种过程,例如激活钙调蛋白。
外部配体可能受酶调节。在神经突触中,乙酰胆碱酯酶将 ACh 降解为可回收的成分;GABA 的降解方式类似。Ca2+ 通过 Na+/Ca2+ 泵主动转运去除。这些不同的配体去除过程有助于调节总浓度并恢复膜不对称性。
内部配体与通道细胞内侧暴露于胞质溶胶的位点结合。示例包括
- 环磷酸腺苷 (cAMP) 和环磷酸鸟苷 (cGMP),两者都被称为“第二信使”。它们是参与启动响应气味和光线的神经元中冲动的通道
允许氯离子和碳酸氢根离子进出细胞的通道受 ATP 调节。患有囊性纤维化的患者的这个通道有缺陷
机械门控离子通道
- 声波弯曲内耳毛细胞的纤毛状突起。它们打开,导致产生大脑解释为声音的神经冲动。
- 牵张感受器细胞的机械变形打开离子通道,导致产生神经冲动。
电压门控通道
这些神经元和肌肉细胞是“可兴奋细胞”。一些通道响应质膜跨膜电荷(以伏特为单位测量)的变化而打开或关闭。一个例子是沿着神经元传递的冲动,膜电压的降低会打开相邻膜部分的钠通道。
载体蛋白
[edit | edit source]载体蛋白是膜结合的转运蛋白,它们与特定的底物结合并改变构象以将底物跨越膜转运。协助扩散是通过载体蛋白实现的。有几种类型的载体蛋白:单向转运蛋白、同向转运蛋白和反向转运蛋白。
单向转运蛋白是一种仅能跨细胞膜移动一种物质的载体蛋白。它们通过一次绑定一个分子并沿着其电化学梯度运输该分子来工作。单向转运蛋白可以通过多种机制进行调节:电压、物理和配体结合。通过电压调节,单向转运蛋白在跨膜电压的临界差值下打开或关闭。对于物理调节,物理压力会导致载体蛋白打开或关闭。最后,对于配体结合调节,配体在细胞内或细胞外侧与单向转运蛋白结合,以诱导载体蛋白的打开或关闭。
其他载体蛋白可以一次跨细胞膜运送多个分子。协同转运蛋白是一种载体蛋白,它同时跨细胞膜以相同方向运输两种或多种不同的分子。相反,逆向转运蛋白是一种载体蛋白,它同时跨细胞膜运输两种或多种不同的分子,其中至少一种分子相对于其他分子以相反方向运输。一般来说,这些载体蛋白至少会将一个分子沿着其电化学梯度运输,而其他分子则会逆着梯度运输。沿着电化学梯度运输的分子将提供驱动力来推动其他分子逆着其电化学梯度运输。这些类型的蛋白质被称为二级转运蛋白或协同转运蛋白。

与被动扩散在膜上无处不在不同,载体蛋白运输的促进扩散最终是基于嵌入的膜蛋白。特别是单向转运和被动扩散,它们都描述了离子跨膜沿浓度梯度运动,它们的最大速率不同:单向转运受限于膜中载体蛋白的位置。
主动运输
[edit | edit source]细胞中的主动运输是指当能量用于跨细胞膜运输分子时发生的现象。被动运输利用有利的浓度梯度来促进离子通过膜的扩散(即从高浓度到低浓度移动蛋白质),而主动运输则需要能量输入,因为所讨论的分子是逆着浓度梯度移动的(即从低浓度到高浓度移动蛋白质)。由于这种类型的运动是“上坡”的,这意味着它在热力学上是不利的,因此需要能量来弥补热力学损失。这确保了所讨论的运输能够成功完成,并且细胞可以获得所需的任何营养,即使这意味着将蛋白质和离子移动到它们的浓度已经相对较高的区域。主动运输中使用的ATP可以被直接或间接使用。对于直接主动运输,一些转运蛋白会直接结合ATP,并利用其水解产生的能量来驱动主动运输,并建立浓度梯度。间接主动运输会利用已经存储在直接泵送离子梯度中的能量。
膜泵
[edit | edit source]细胞利用膜泵来帮助完成主动运输。泵可以将自由能转换为不同的形式,这取决于细胞在特定时间需要哪种形式。这种特性使膜泵成为介导主动运输的便捷选择,因为它们可以提供启动运输所需的能量。细胞使用的两种主要泵类型是P型ATP酶和ATP结合盒转运蛋白(ABC)。这两种泵都由ATP驱动,ATP是细胞能量的更常见形式之一。这些泵执行主动运输的一种方法是结合ATP。这种结合,接着是水解,会导致泵发生构象变化,使结合的离子能够跨细胞膜运输。这些泵还可以使用主动运输来建立有利的浓度梯度,用于独立的运输过程。例如,一个泵可以通过对特定离子执行主动运输来建立给定的浓度梯度,然后另一个泵可以通过促进离子沿着浓度梯度扩散来利用这个新的浓度梯度。因此,细胞可以将主动运输与被动运输相结合(就像它将吸热反应与放热反应相结合一样),以便有效地利用一个过程的结果来驱动另一个过程完成。
Na+-K+泵
[edit | edit source]
Na+-K+泵,也称为Na+-K+ATP酶,是一种酶,细胞用它来控制其细胞内介质中的离子梯度。顾名思义,它处理的离子是钾离子和钠离子,它们是生物系统中两种最常见的离子。在这种情况下,Na+-K+泵水解ATP以提供将Na+主动运输出细胞并将K+运输入细胞所需的能量。出于这个原因,大多数动物细胞中的钾离子浓度往往明显高于钠离子浓度;细胞需要这种浓度才能促进各种细胞过程。Na+-K+泵通过产生必要的离子梯度来帮助其维持这种浓度。http://www.youtube.com/watch?v=bGJIvEb6x6w&feature=related
其他两种与Na+-K+泵同源的酶“泵”是Ca2+ATP酶和H+-K+ATP酶。Ca2+ATP酶负责将钙离子(Ca2+)从正常组织细胞的细胞质中运输到肌肉细胞的肌浆网中。肌肉细胞需要钙离子才能以最佳效率发挥作用;因此,这种泵确保它们获得足够的钙离子以满足这一需求。H+-K+ATP酶将大量的质子(H+)泵入胃的胃液中,以保持pH值低于1.0。如此低的pH值是必要的,因为胃负责消化进入的所有食物和液体;因此,它的胃液需要足够酸性才能溶解和分解任何需要消化的东西。
上述三种泵都属于一个称为P型ATP酶的家族,之所以这样称呼,是因为它们在与ATP反应过程中都会形成磷酸化中间体。在P型ATP酶中存在数百种已知的这种泵同源物,每个泵在维持细胞的功能方面都发挥着确定的作用。
多药耐药(MDR)泵
[edit | edit source]MDR泵由ATP激活,存在于细菌和癌细胞等微生物中。多药耐药(MDR)泵由穿透细胞表面膜的大蛋白组成。它们的工作原理是有效监测和阻止不需要的化学物质进入细胞。因此,微生物具有使用MDR泵进行自我防御的能力。MDR泵还可以阻止抗生素进入细菌,阻止化疗药物进入癌细胞。此外,它们还用于将可能危及细菌的物质排出体外。用MDR抑制剂联合使用抗生素可能是一种规避细菌中MDR泵的方法。这解释了细菌抵御抗生素的超凡能力。MDR泵可以在人类中找到,它们在帮助药物到达需要到达的地方方面发挥着多种作用。它们在大脑、消化道、肝脏和肾脏的膜中也很重要,因为它们通过膜将激素移入移出细胞(Medicines by Design 15)。
例如,AcrB是革兰氏阴性菌中一种有效的MDR。它通过其三个不对称的亚基发挥作用,每个亚基都以与泵中功能相对应的特定构象存在。三个阶段分别是进入、结合和排出。在进入阶段,底物进入亚基的前庭,结合口袋仍然保持完整。在结合阶段,底物仍然留在前庭中,但结合口袋扩大以更好地容纳底物。最后,在排出阶段,底物通过去除中心螺旋而退出。AcrB用于将多种药物从膜中排出,其中一些包括防腐剂、有毒化合物和抗生素。
囊泡
[edit | edit source]囊泡只是细胞中的一种液体气泡。具体来说,囊泡是一种膜结合囊,有助于细胞废物或细胞产物的运输和储存、代谢和浮力控制。包围囊泡的膜与细胞的质膜具有许多共同特征。因此,囊泡可以与膜融合,以丢弃其内容物。
运输囊泡
这些只是具有运输功能的特定类型的囊泡。它们在粗面内质网和高尔基体之间移动分子、产物等。两种类型的蛋白质是在粗面内质网上的核糖体上合成的。从这里,运输囊泡将新蛋白质带到高尔基体。在高尔基体中,蛋白质会老化和成熟,以便被运输到最终目的地。蛋白质始终与运输囊泡一起在细胞内部移动。
脂质囊泡
也称为脂质体,这些囊泡是水性隔室,被脂质双层包围。这些囊泡用于监测膜渗透性和将化学物质递送至细胞。脂质囊泡有助于确定膜对离子和平极分子的不透性水平。离子和平极分子被困在脂质体的含水隔室中。膜转运过程中从囊泡的内部隔室流向外部溶液的流速决定了膜对内部含水隔室中所含离子和平极分子的不透性。脂质体是在磷脂存在下用超声波处理形成的,其中包含离子、极性分子或水溶性物质。
有被囊泡:
这些是当新出现的芽从细胞膜上分离时形成的囊泡。根据囊泡的形成方式,外层包被的形成可能会形成囊泡,而在其他情况下,则需要其他酶来形成囊泡。它是一种细胞内结构。囊泡的外表面被一层网格状或笼状的网格蛋白网格覆盖。
网格蛋白 是一种在细胞膜胞质侧形成网格状覆盖物的蛋白质。这些胞质侧被称为包被坑,是形成包被囊泡的第一阶段。它通过制造称为三叉蛋白的亚基来形成。三叉蛋白是一个三叉分子,具有三个 N 末端区域。它们被称为重链,重量约为 192kDa,与重量约为 30kDa 的轻链结合。坑的内陷发生在内吞作用的最初阶段,并导致形成网格蛋白包被囊泡。网格蛋白可以自发组装,它在变形萌芽囊泡中起着重要作用。虽然网格蛋白是变形的主要参与者,但还有一些辅助蛋白帮助组装和拆卸包被。
COP I 是另一种在蛋白质转运过程中包被囊泡的蛋白质。然而,这种囊泡包被将蛋白质从高尔基体运输到粗面内质网。由于这与正常运输方向相反,因此被称为逆向运输。蛋白质包被由具有 7 个独特亚基的大型蛋白质亚复合物组成。
这种蛋白质被称为 ADP 核糖基化因子依赖性衔接蛋白。这基本上意味着它们是囊泡生物发生的调节剂。它们还帮助选择用于转运蛋白的蛋白质。
COP II 与 COP I 非常相似,因为它转运蛋白质,但 COP II 将蛋白质从粗面内质网运输到高尔基体,被称为顺向运输。COP II 具有由 4 个独特的蛋白质亚基组成的包被。COP II 具有三个不同的结合位点,可以与其他蛋白质形成复合体。
COP I 和 COP II 在膜转运中都非常活跃。它们执行选择蛋白质正确货物和将磷脂双分子层形状改变成正确的芽和囊泡的必要任务。
顺向和逆向运输相互抵消,以帮助保持膜和分泌物的流动平衡。为了维持不同途径中驻留蛋白的等量,不断进行着循环利用。
半透膜通常对跨脂质双分子层的电荷和电压敏感。请记住,膜是带电实体,因此在膜上施加电荷可能会引起反应,例如动作电位。动作电位通常在膜因电压升高或降低而去极化后,在轴突起始段产生。当膜电位升高时,膜中称为电压门控离子通道的整合蛋白开始打开,允许离子进入细胞。虽然某些离子通道允许离子进入细胞,但其他通道允许离子流出细胞。钠钾泵就是最典型的例子。因此,由于钠离子流入细胞,而钾离子流出细胞,发生去极化,即正常的膜电位(称为静息电位)被扰乱。请注意,动作电位是全或无的,这意味着动作电位的发生不依赖于刺激的大小。单个动作电位可以触发膜上的多个动作电位,从而传播信号。
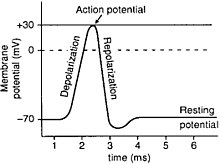

只有某些类型的细胞具有动作电位的活性。最重要的细胞是神经元。神经元是神经系统中的一种细胞,它通过动作电位的电子兴奋性产生信息并发送信号。轴突起始段是神经元连接细胞与轴突的部分。该区域具有许多电压激活的离子通道,被认为是产生去极化(产生动作电位)的关键因素。

神经递质是放大或控制神经元与另一个细胞之间信号的化学物质。当神经递质释放到突触间隙时,它们会与受体结合并引起动作电位,然后可以触发其他神经元也这样做,从而在一组执行特定过程的神经元中产生能量激增。整个过程被称为神经传递。动作电位可以通过间隙连接(这些细胞的直接连接)从一个细胞传递到相邻的细胞。通道和其他膜蛋白确保动作电位仅朝一个方向传播。一些细胞不需要刺激即可触发动作电位,而其他细胞则需要外部刺激。例如,心脏的起搏细胞维持着一种节奏,这种节奏可以通过外部刺激(例如对身体的电击)来改变和改变。而像你的眼睛中的感光神经元这样的感觉神经元,会被外部来源兴奋,然后引发动作电位。耳朵中对声音敏感的细胞也是如此。
一些化学物质通过竞争性地与受体结合来阻断神经递质的结合。诸如箭毒或阿托品之类的物质被称为拮抗剂,它们与神经递质(特别是乙酰胆碱 (ACh))竞争,与之结合并阻止配体门控通道打开并允许离子流动,从而阻止动作电位的产生。在自然环境中,这种竞争性抑制会导致瘫痪和死亡。在受控环境中,这些拮抗剂可用于在手术过程中防止肌肉痉挛或抽搐。
Alberts, B., Bray, D., Lewis, J., Raff, M. and Roberts, K. 1989. The Cell, 2nd Ed.
Berg, J.M, Tymoczko, J.L. and Stryer, L. Biochemistry. 6th ed. New York: W.H. Freeman and Company, 2007. Print.
Carruthers, Anthony. 1990. “Facilitated diffusion of glucose.” Physiological Review, vol 70-4: 1135-76. PubMedhost(accessed November 16, 2009).
Silverthorn, Human Physiology 5th Edition
Purves et al., Neuroscience, 4th Edition
http://www.biologie.uni-hamburg.de/lehre/bza/kanal/porin/eporin.htm#
http://www.answers.com/topic/ionophore
http://www.ncbi.nlm.nih.gov/bookshelf/br.fcgi?book=mcb&part=A4038
Lodish, Harvey, et al. 2003. Molecular Cell Biology 5th Edition. pages 708-710. W. H. Freeman.
http://en.wikipedia.org/wiki/ATP-binding_cassette_transporter#Mechanism_of_Transport

