结构生物化学/促胰液素
人体内存在着许多激素,它们调节和控制着身体机能。其中,促胰液素是关键成员之一。促胰液素是一种调节十二指肠正常分泌并调节人体稳态的激素。十二指肠位于人体小肠内,位于小肠上皮内衬的肠腺中。在这里,可以找到产生促胰液素的 S 细胞。发现促胰液素参与人体多个功能器官(如肾脏)的渗透压调节的关键功能。促胰液素功能的更具体特征是其调节十二指肠内容物 pH 值的能力。这种功能可以通过促胰液素激素调节胃酸的特定分泌并利用各种化学缓冲剂控制其 pH 特性来实现。通常,所使用的化学缓冲剂必须是人体能够随时获得的,不需要额外摄入营养物质。这种特定的促胰液素用来缓冲 pH 的化合物是碳酸氢盐。碳酸氢盐可以从胰腺内的梭形细胞(称为中心腺泡细胞)中找到。除了在胰腺中被发现之外,碳酸氢盐也可以在插管小管中找到。关于促胰液素的一个有趣的事实是,它们是第一个被发现并正确识别的激素。
促胰液素最早是在 20 世纪初由两位英国生理学家恩斯特·斯塔林和威廉·贝利斯发现的。他们项目的实验设计是针对神经系统如何响应和调节消化过程。由于早期的发现,他们知道胰腺是分泌帮助消化化合物的关键组成部分。当食物通过幽门括约肌进入十二指肠时,这个过程就会发生。这两位科学家在这个实验中能够反驳早期的发现,当时他们发现神经系统实际上并没有控制消化功能。相反,他们发现现在被称为促胰液素的物质是在肠道中产生的,它实际上是控制消化系统的因素。
促胰液素的化学组成涉及几个关键成分。该结构首先是由前体产生的,前体包含一个间隔区、促胰液素激素本身、一个 N 端信号肽和一个包含 72 个氨基酸的 C 端肽。整个激素前体总共包含 120 个氨基酸;然而,促胰液素部分实际上只位于第 28 到 54 个残基之间。除了前体肽之外,还包含成熟的促胰液素肽。该肽由 27 个氨基酸残基组成,并以线性序列排列。其特征是分子量为 3055。这种成熟线性促胰液素肽的 3D 结构与其一些常见的化合物具有相同的结构。与胰高血糖素、葡萄糖依赖性胰岛素促分泌肽和血管活性肠肽类似,促胰液素呈现螺旋状。这在氨基酸 5 到 13 的位置最为突出。这种螺旋化学结构的氨基酸分解如下。成熟促胰液素中的 7 个氨基酸残基也可以在血管活性肠肽中找到,14 个氨基酸残基可以在与胰高血糖素中发现的那些氨基酸残基相似的排列中找到,而促胰液素中的 10 个氨基酸残基可以在与葡萄糖依赖性胰岛素促分泌肽中相对应的位点找到。除了前体和成熟的促胰液素之外。促胰液素激素的另一个特殊特性是它具有一个酰胺化的羧基末端氨基酸,即缬氨酸。
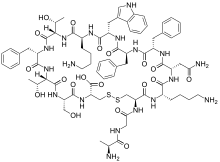
因此,促胰液素激素的相应序列为:H2N–His-Ser-Asp-Gly-Thr-Phe-Thr-Ser-Glu-Leu-Ser-Arg-Leu-Arg-Asp-Ser-Ala-Arg-Leu-Gln-Arg-Leu-Leu-Gln-Gly-Leu-Val–CONH2。
T2SS:II 型分泌系统有助于调节水解酶的数量,以及将毒素从周质空间向细胞外排出。已知携带 T2SS 的细菌是大肠杆菌和霍乱弧菌,这两种细菌以霍乱和腹泻疾病而闻名。与这些疾病相关的毒素与 T2SS 蛋白相关。
T4PS:IV 型菌毛系统是一种促胰液素,它有助于产生和拆卸在致病性/环境细菌中发现的细胞外纤维。这种促胰液素由许多类型的 IV 型菌毛组成;T4aP 和 T4bP。这些 IV 型菌毛主要负责运动、蛋白质分泌以及将促胰液素附着到细胞上。一些具有 T4PS 的细菌是淋病奈瑟菌和铜绿假单胞菌。
T3SS:III 型分泌系统是一种将病毒蛋白转移到细胞质的途径。T3SS 也被称为注射体,它使病原体能够将效应因子转移到宿主体内,并直接改变正常的细胞行为。T3SS 的病原体反应会导致生理细胞反应,例如炎症、吞噬作用,甚至细胞凋亡。利用 T3SS 的细菌是沙门氏菌、肠致病性大肠杆菌和弗氏志贺氏菌。
促胰液素激素首先在 S 细胞中产生。具体来说,是在该细胞的细胞质分泌颗粒部分。此外,S 细胞也可以在覆盖着上皮的粘膜中找到,上皮是一种在吸收和分泌中起关键作用的产物。此外,这些衬里也可以在十二指肠以及小肠的空肠部分找到。然而,小肠中的 S 细胞和促胰液素数量在这里较小。
根据不同物种的不同,促胰液素通常会根据十二指肠环境的 pH 范围产生不同的反应。一般来说,当十二指肠的 pH 值达到约 2 到 5 的酸性功能时,促胰液素激素就会被激活并释放到循环系统中。促胰液素释放的另一种情况也可能发生在肠腔内。然而,这两种情况都是对 pH 值变化到较低范围的反应。除了 pH 值控制之外,当氨基酸残基分解产生包含在小肠(通常在上部区域)的粘膜中的产物时,促胰液素分泌也可以最大化。

十二指肠通常会根据其腔室中盐酸 (HCl) 的含量来创造其酸性环境。半消化的食物,或称食糜,会从胃中喷射出来,进入十二指肠。因此,盐酸会穿过连接胃和十二指肠的胃部区域,该区域被称为幽门括约肌。一旦 HCl 进入十二指肠,它就会酸化环境并导致 pH 值下降,进而激活促胰液素的释放。一旦促胰液素最终释放,它就会用于靶向消化和内分泌系统中的腺体器官,即胰腺。一旦胰腺接收到一定量的胰岛素,该器官就可以产生并排出富含碳酸氢盐的体液。然后,这种溶液会流过相应的肠道。胰腺需要产生碳酸氢盐,因为这种多原子离子产生的单个离子可用于中和已经存在的酸。有了碳酸氢盐的存在,身体现在可以使用它来创造有利于 pH 值的环境,以便它可以执行肠道中消化酶的作用。拥有碳酸氢盐的关键特征是中和酸并防止酸灼伤。胰腺还可以作为对促胰液素的反应引入碳酸氢盐,通过产生脂肪酸和各种胆汁盐。这两种化合物反过来都可以产生碳酸氢盐作为产物,并与最初的一组碳酸氢盐结合,并放入小肠中。抑制促胰液素分泌的一种方法是添加一类药物,这些药物用于阻断胃部细胞中组胺的作用。这些被称为 H2 受体拮抗剂。这些化合物通过减少胃酸分泌而起作用。由于十二指肠中胃酸含量降低,pH 值无法保持在较低水平。因此,一旦十二指肠的 pH 值升至 4.5-5 以上,促胰液素将不再产生和释放。相应的器官功能可以成功地关闭。
促胰液素激素的主要功能是增加胆汁以及胰腺管上皮细胞中的碳酸氢盐溶液。驻扎在胰腺中的细胞具有识别促胰液素激素的受体,一旦促胰液素到达其质膜。一旦激素附着在受体上,它就可以积极地激发并产生腺苷酸环化酶活性。腺苷酸环化酶活性用于将三磷酸腺苷,ATP,转化为环腺苷一磷酸或 cAMP。换句话说,从一个能量储存分子到一个在生物过程中重要的信使。值得注意的是,环磷酸腺苷被用作二级信使,以在整个细胞中传递信号并促进释放更多碳酸盐离子的增加。此外,产生更多环磷酸腺苷可用于促进胰腺的生长和结构稳定。

促胰液素的其他功能包括抵消胰腺产生的血糖浓度峰值增加的影响。当胰腺减少胰岛素的释放时,人体内的血糖浓度开始无序地飙升。通过向体内释放促胰液素,它可以通过触发胰岛素的释放来推迟和消除此类血糖浓度峰值的影响。
促胰液素在人体中执行的另一个功能是,它可以积极地延迟和停止胃中胃泌素的释放。促胰液素可以执行此功能,因为它可以减少胃分泌的酸,并抑制 G 细胞中胃泌素的释放。这种功能有助于中和进入十二指肠的消化产物的 pH 值。据表明,酶在最佳状态下产生消化功能,即略带碱性的 pH 值。
此外,促胰液素在人体中起到的作用是,它可以积极地增加胃中释放胃蛋白酶原、凝乳酶和胃脂肪酶的细胞(即主细胞)中胃蛋白酶的分泌。这种对主细胞的积极刺激可以帮助在食物消化过程中分解蛋白质。促胰液素可以实现此功能,因为它刺激释放生长抑素释放抑制因子和胰高血糖素。
最后,除了维持通过十二指肠器官传递的额外酸性食糜外,促胰液素还具有其他功能。其中之一是促胰液素改善了肽激素胆囊收缩素的作用,并诱导胰腺分泌消化过程中所需的额外酶。促胰液素在此功能中产生的另一种作用是,它还可以增加胆囊中产生的胆汁,胆囊是一个小的器官,有助于脂肪消化。
促胰液素在行业中有多种用途。促胰液素发挥的一种独特功能是,它可以增加人类的胰腺分泌。这在医学领域极其重要,因为监测胰腺功能和进行测试的科学家需要促胰液素激素产生的放大效应。可以使用多种方法将促胰液素引入体内。促胰液素可以引入人体的两个主要途径是直接注射到十二指肠或通过正常注射。某些促胰液素测试的结果已被用于证明并提供对胰腺异常的见解。最后,据表明,促胰液素可以为自闭症和其他基于大脑的疾病提供潜在的治疗方法。
促胰液素有助于将蛋白质分泌到革兰氏阴性菌(能够获得抗生素耐药性的细菌[9])的细胞外环境中。在细菌中,它们构成三个不同的外膜通道。[10]
T2SS 由三个亚基组成:外膜复合体、丝状假菌毛和内膜平台。这些负责从周质(质膜和与细胞质相邻的膜之间的区域[11])分泌毒素。
分泌发生在两个步骤中。蛋白质与 N 端信号肽一起产生。接着去除信号肽,以及成熟蛋白质的折叠和释放到周质中。它们可能在通过 T2SS 穿过膜分泌之前进行进一步的修饰。[13]
T4PS 通过组装和拆卸细菌表面的纤维来帮助细菌在表面移动,而无需使用鞭毛。这些系统由两个菌毛亚类组成:T4aP 和 T4bP。[10]
纤维是 α 螺旋周围的三层螺旋结构,周围环绕着 β 片。这两层内层被表面的 C 端区域覆盖。N 端氨基酸序列形成最里面的 α 螺旋螺旋。这种疏水性堆积和 α 螺旋的灵活性使菌毛能够弯曲并采用扭曲或捆绑的构象。β 片的中间层从一个单体到另一个单体是连续的,并且 β 片氢键提供了大部分稳定性。人们普遍认为,菌毛从其底部组装起来,因为在细胞膜中发现了菌毛蛋白库。由于纤维中心没有通道,因此排除了从尖端组装。[14]
这些也被称为注射体。它们用于转运细菌效应子。[10]
它具有基底体、针状结构和尖端。[12]
尖端被细菌分泌到周围环境中,并与宿主细胞接触。针状结构在宿主细胞膜中形成一个孔。然后,效应蛋白可以通过针状结构进入宿主细胞。[12] 这最终会导致细菌在宿主体内传播。
秘密蛋白通常由外膜中的脂蛋白(称为导向蛋白)产生。一个已知的例子是 MxiM,一种常见于 T3SS 中的导向蛋白。MxiM 主要由 β 折叠片组成,并含有一个 α 螺旋,它们共同形成锥形结构。MxiM β 折叠片的疏水部分充当脂类或自身(N 端可以与 C 端结合,形成环状结构)的结合位点。形成后,导向蛋白与外膜结合,并组装秘密蛋白。导向蛋白之间(或与其他脂类或导向蛋白)的相互作用方式有助于决定其结构,从而影响其功能。不同结构的导向蛋白会导致形成特定功能的不同秘密蛋白。
另一个值得注意的例子是导向蛋白 PilF,它对于产生 PilQ 至关重要,PilQ 是一种常见于铜绿假单胞菌中的 T4PS 秘密蛋白。PilF 通常与来自类似细菌脑膜炎奈瑟菌的另一个导向蛋白 PilW 结合,从而形成多聚秘密蛋白。就形式决定功能而言,这两个导向蛋白在表面都具有凹形结构,许多研究人员认为这可能是生产 T4aP 的潜在结合位点,T4aP 是产生 T4PS 秘密蛋白所必需的。
在导向蛋白产生不同的秘密蛋白系统后,这些分泌系统会与细胞的内膜结合并形成秘密蛋白多聚体。这些秘密蛋白多聚体由许多秘密蛋白组成,这些秘密蛋白共同形成特定的秘密蛋白系统。此类秘密蛋白的例子包括 GspCEpsC 和 GspMEspM,它们是两种常见于 T2SS 系统中的绿色荧光蛋白。已知这两种蛋白有助于秘密蛋白系统在膜内的定位以及整个系统的实际产生。
5. http://special.edschool.virginia.edu/information/secretin.html
6. http://www.drugs.com/ppa/secretin.html
7. http://www.medicinenet.com/secretin/supplements-vitamins.htm
8. http://www.nlm.nih.gov/medlineplus/ency/article/003892.htm
9. http://www.cdc.gov/hai/organisms/gram-negative-bacteria.html
10. http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3155655/
11. http://www.merriam-webster.com/dictionary/periplasm
12. http://www.nature.com/nchembio/journal/v8/n1/fig_tab/nchembio.741_F1.html
13. http://onlinelibrary.wiley.com/doi/10.1046/j.1365-2958.2001.02403.x/full
14.http://onlinelibrary.wiley.com/doi/10.1046/j.1365-2958.1999.01339.x/full
15. http://www.sciencedirect.com/science/article/pii/S0968000411000557
