人体营养学基础/维生素 D
- 维生素 D 传统上被称为抗佝偻病因子或阳光维生素。
- 维生素 D 独一无二,因为它是由身体合成的维生素,并且它起着激素的作用。
- 除了在钙稳态和骨骼矿物质代谢中发挥关键作用外,维生素 D 内分泌系统现在被公认为在细胞分化、抑制细胞生长以及免疫调节方面的一系列基本生物学功能中发挥着重要作用。
- 它是一种调节复杂基因组功能系统的类固醇,在预防肿瘤转化中起作用。
- 最近来自遗传、营养和流行病学研究的证据将维生素 D 内分泌系统与高血压、肌病、感染倾向、自身免疫性疾病和癌症等疾病联系起来。
- 维生素 D 调节细胞周期蛋白的转录,这会减少许多专门细胞(破骨细胞前体、肠上皮细胞、角质形成细胞)的细胞增殖并增加细胞分化。[1]
维生素 D 不是必需的营养素,尽管它被认为是维生素,但它更像是一种激素。维生素 D 需要被激活才能发挥作用。这可以通过两种方式之一来完成:通过阳光的紫外线辐射或通过食用食物。在阳光充足的情况下,维生素 D 可以合成,而无需直接从食物中获得(Whitney 11.2)。这种从阳光中合成维生素 D 的过程可以在人类的表观遗传学中看到。从旧石器时代起,维生素 D 就可能发生了潜在的改变。在那个时代,人们生活在户外,没有穿任何衣服来遮挡皮肤免受阳光照射。那么,我们现在接收到的阳光量与过去相比到底有什么不同呢?阳光照射是激活维生素 D 胆固醇的必要因素,但所需的精确紫外线阳光量尚不清楚。据说每周三次,每次五到十五分钟的阳光照射到脸部、手臂、腿部或背部,可能足以吸收足够的维生素 D(克利夫兰诊所健康事实说明书)。可能影响所需阳光照射量的一些因素包括年龄、肤色和地理位置。老年人、深色皮肤的人以及生活在北部气候的人可能需要更多的阳光照射(克利夫兰诊所健康事实说明书)。
维生素 D 可以少量地存在于一些食物中,例如
- 油性鱼类(鲑鱼、沙丁鱼、鲭鱼、金枪鱼)
- 鸡蛋
- 奶粉
- 早餐麦片
- 强化脂肪涂抹酱(人造黄油)
- 奶酪
维生素 D 的浓缩食物来源包括沙丁鱼、牛奶、山羊奶、香菇和鸡蛋。在鲑鱼中,野生捕捞的鱼的维生素 D 平均含量明显高于非有机养殖的鱼。[2]
除了食物之外,你还可以从阳光中获得维生素 D,这是由于皮肤在阳光中的紫外线和人体化学物质之间发生反应造成的。
"维生素 D" 这个词指的是这种维生素的几种不同形式。两种形式对人类很重要:麦角钙化醇(维生素 D2)和胆钙化醇(维生素 D3)。维生素 D2 由植物合成。维生素 D3 是当人类皮肤暴露在阳光中的紫外线 B(UVB)射线下时在皮肤中合成的。食物中可能会添加维生素 D2 或 D3。
维生素 D 的形式
两种主要形式是维生素 D2 或麦角钙化醇,以及维生素 D3 或胆钙化醇;没有下标的维生素 D 指的是 D2 或 D3 或两者。这些统称为钙化醇。[8] 维生素 D2 在 1931 年被化学鉴定。1935 年,维生素 D3 的化学结构被确定,并被证明是由 7-脱氢胆固醇的紫外线照射产生的。(9)
名称化学成分结构
维生素 D1 麦角钙化醇与光照异构体的混合物,摩尔比 1:1
维生素 D2 麦角钙化醇(由麦角甾醇制成)
维生素 D3 胆钙化醇(由皮肤中的 7-脱氢胆固醇制成)。
维生素 D4 22-二氢麦角钙化醇
维生素 D5 谷甾醇钙化醇(由 7-脱氢谷甾醇制成)
维生素 D 在我们身体中的主要功能是促进胃中钙和磷的利用和吸收,从而维持骨骼和牙齿的健康。维生素 D 的其他作用包括促进细胞生长和减少体内炎症。
- 帮助优化钙代谢
- 帮助优化磷代谢
- 帮助预防 2 型糖尿病、胰岛素抵抗、高血压、心脏病、充血性心力衰竭和中风
- 帮助预防跌倒和肌肉无力
- 帮助预防骨质疏松症,同时保持骨骼完整性
- 帮助调节胰岛素活性及血糖平衡
- 帮助调节免疫系统反应
- 帮助调节肌肉成分和肌肉功能
- 帮助调节血压
- 降低过度炎症的风险
- 降低某些细菌感染的风险
- 支持认知功能,特别是在老年人中
- 支持情绪稳定,特别是在老年人中
- 帮助预防慢性疲劳
- 帮助预防以下类型的癌症:膀胱癌、乳腺癌、结肠癌、卵巢癌、前列腺癌和直肠癌
参考文献 • http://www.nutristrategy.com/nutrition/vitamind.htm
- http://ods.od.nih.gov/factsheets/VitaminD-HealthProfessional/
- http://www.whfoods.com/genpage.php?tname=nutrient&dbid=110
皮肤中的生成
在皮肤的表皮层中,生成量在基底层和棘层中最高。维生素 D3(胆钙化醇)是由皮肤中的 7-脱氢胆固醇通过光化学反应产生的。7-脱氢胆固醇在大多数脊椎动物(包括人类)的皮肤中大量产生,每 30 分钟全身暴露于阳光下会产生 10,000 至 20,000 国际单位的维生素 D。(10) 7-脱氢胆固醇与 270 至 300 纳米波长的 UVB 型紫外线发生反应,合成峰值出现在 295 至 297 纳米之间。[11] 当紫外线指数大于 3 时,阳光中存在这些波长,以及晒黑床中使用的紫外线灯发出的光(主要产生 UVA 光谱中的紫外线,但通常产生 4% 至 10% 的总紫外线发射为 UVB)。当紫外线指数大于 3 时,这种情况在热带地区每天都会发生,在温带地区春季和夏季每天都会发生,而在北极圈内几乎从未发生,维生素 D3 可以在皮肤中生成。即使紫外线指数足够高,通过窗户照射的光线也不足以生成维生素 D,因为紫外线无法穿透窗户。[12] 根据 UVB 射线的强度和照射的分钟数,皮肤中会形成平衡,维生素 D 的降解速度与生成速度一样快。[13] 皮肤由两层主要层组成:内部层称为真皮,主要由结缔组织组成,以及外部、较薄的表皮。脚掌和手掌的厚表皮由五层组成;从外到内分别是:角质层、透明层、颗粒层、棘层和基底层。维生素 D 在最里面的两层(基底层和棘层)中生成。裸鼹鼠似乎天生就缺乏胆钙化醇,因为血清 25-羟基维生素 D 水平检测不到。[14] 在一些动物中,毛皮或羽毛的存在阻挡了紫外线到达皮肤。在鸟类和毛皮动物中,维生素 D 是由皮肤的油性分泌物产生的,这些分泌物沉积在羽毛或毛皮上,并在梳理过程中口服获得。[15]
维生素 D 在我们身体中的作用:
维生素 D 虽然被称为维生素,但实际上,当它处于活性形式时,它是一种激素。维生素 D 包含一种结合蛋白,将其运输到必要的生命器官,主要是骨骼、肾脏和肠道(Whitney & Rolfes, 2013)。维生素 D 在我们体内最主要的功效之一是骨骼健康,特别是它帮助吸收钙和磷以及调节它们的血液浓度。随着这些矿物质被吸收和沉积到我们体内的骨骼中,骨骼逐渐变得更加强壮,并获得骨骼健康所必需的密度。根据惠特尼在 2013 年的文字记载,富含维生素 D 的饮食促进消化道对钙和磷的吸收,但维生素 D 也会在饮食不足的情况下,从肾脏等其他部位提供必要的矿物质,并通过从骨骼中动员来补充。根据许多研究,除了骨骼健康之外,维生素 D 对预防和治疗“糖尿病、心脏病、高血压和多发性硬化症”也至关重要(克利夫兰诊所,2015)。维生素 D 还被发现有助于预防乳腺癌、结肠癌和前列腺癌。维生素 D 在调节免疫和神经肌肉系统方面也同样重要(DeNoon)。
维生素 D 有助于预防 II 型糖尿病,这是一种身体在血液中积累糖分的疾病。II 型糖尿病通常在 40 岁后才发展,但也可能更早出现。维生素 D 及其在调节钙方面的作用有助于控制血液中的糖分。胰岛素是由胰腺中的胰岛β细胞产生的,而患有 II 型糖尿病的人,其胰岛β细胞的功能不佳。研究表明,β细胞中存在一些受体,这些受体只能被维生素 D 激活。因此,假设维生素 D 可以帮助改善胰岛素的产生,从而使身体能够将糖转化为葡萄糖。此外,钙有助于调节胰岛素的释放。因此,充足的维生素 D 水平会提高钙的生物利用度,进而有助于胰岛素的释放(Chiu,2004)。维生素 D 还有助于预防心脏病和心力衰竭。冠心病是指血液供应到心脏受阻,而充血性心力衰竭是指心脏无法向身体泵出足够的血液。在这两种情况下,高水平的维生素 D 都可以降低心血管疾病的风险。这是因为维生素 D 会降低糖尿病(如上所述)和高血压。维生素 D 还可以帮助减少动脉壁的增厚、呼吸道感染和炎症(Anderson,2010)。
维生素 D 还会与我们的皮肤细胞在阳光的照射下协同作用。当阳光中的特定波长的紫外线 B 光照射到我们的皮肤细胞时,皮肤细胞中的一个分子 7-脱氢胆固醇可以转化为维生素 D 的初始形式,即胆钙化醇(世界最健康的食物)。影响维生素 D 产生的因素很多,因此很难准确地说出通过皮肤细胞与阳光的相互作用能产生多少维生素 D。维生素 D 在人体的免疫力方面也至关重要,因为它参与白细胞的成熟,帮助身体抵抗感染。最近的研究发现,呼吸道感染与低维生素 D 存在关联(世界最健康的食物)。随着年龄的增长,我们的骨骼会随着时间的推移而变得更加脆弱,许多老年人会患上骨质疏松症、骨质流失以及肌肉整体无力等疾病,这是因为随着年龄的增长,激活维生素 D 变得更加困难。维生素 D 对调节细胞生长的基因活性也十分有益,这可以用于治疗诸如“代谢综合征、2 型糖尿病、结核病、炎症、多发性硬化症、黄斑变性、高血压以及某些癌症”等疾病(Whitney & Rolfes,2013)。维生素 D 激素使成骨细胞产生一种特殊的配体,然后刺激破骨细胞生成,从而使骨骼发生重塑。由于这一点,维生素 D 在“当饮食中缺乏钙时,使人体能够从骨骼中动员钙”方面发挥着至关重要的作用(DeLuca,2004)。总而言之,维生素 D 具有多种功能,其中最重要的是它在骨骼健康、免疫、皮肤、血糖以及预防多种疾病方面的作用。
参考文献
[edit | edit source]- ↑ Harinarayanan, C., & Shashank, R. J. (2009). Vitamin d status in india – its implications and remedial measures. In C. JAPI (Ed.), JAPI-review article (Vol. 57, pp. 40-49). India: JAPI. doi:www.japi.org
- ↑ http://www.whfoods.com/genpage.php?tname=nutrient&dbid=110
- DeLuca, H. (2004). Overview of general physiologic features and functions of vitamin D1,2,3,4. The American Journal of Clinical Nutrition. Retrieved December 1, 2015, from http://ajcn.nutrition.org/content/80/6/1689S.full
- DeNoon, J. Daniel (n.d.). Vitamin D FAQ: Why You Need Vitamin D. Retrieved December 1, 2015, from http://www.webmd.com/osteoporosis/features/the-truth-about-vitamin-d-why-you-need-vitamin-d
- The Role Of Vitamin D In Your Health. (2015). Retrieved December 1, 2015, fromhttps://my.clevelandclinic.org/health/diseases_conditions/hic_Osteoporosis/hic_The_role_of_vitamin_D_in_your_health
- The World's Healthiest Foods. (n.d.). Vitamin D. Retrieved 2015, from http://www.whfoods.com/genpage.php?tname=nutrient&dbid=110#function
- Whitney, E., & Rolfes, S. (2013). Understanding Nutrition (14th ed.). Belmont, CA: Cengage Learning.
作用机制
[edit | edit source]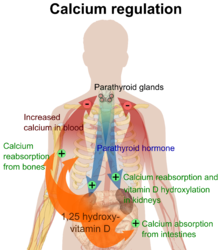
维生素 D 通过血液循环到达肝脏,在那里被转化为前激素骨化三醇。循环的骨化三醇可以被转化为维生素 D 的生物活性形式骨化三醇,转化发生在肾脏或免疫系统的单核细胞-巨噬细胞中。当由单核细胞-巨噬细胞合成时,骨化三醇在局部起细胞因子的作用,防御身体免受微生物入侵者。[16][2] 肾脏进行最后的转化步骤后,骨化三醇(维生素 D 的生理活性形式)被释放到循环中。通过与维生素 D 结合蛋白 (VDBP) 结合,VDBP 是血浆中的一种载体蛋白,骨化三醇被运输到各种靶器官。[5][3]
骨化三醇通过与维生素 D 受体 (VDR) 结合来介导其生物学效应,VDR 主要位于靶细胞的细胞核中。[5][3] 骨化三醇与 VDR 的结合使 VDR 能够作为转录因子,调节参与肠道中钙吸收的转运蛋白(如 TRPV6 和钙结合蛋白)的基因表达。[17][4] 维生素 D 受体属于类固醇/甲状腺激素受体的核受体超家族,VDR 由大多数器官的细胞表达,包括大脑、心脏、皮肤、性腺、前列腺和乳腺。VDR 在肠道、骨骼、肾脏和甲状旁腺细胞中的激活导致维持血液中钙和磷的水平(在甲状旁腺激素和降钙素的帮助下),并维持骨骼含量。[18]([5]) 维生素 D 增加了肾上腺髓质细胞中羟化酶基因的表达。它还参与神经营养因子的生物合成、一氧化氮合酶的合成以及谷胱甘肽水平的提高。[19]([6])
众所周知,VDR 参与细胞增殖和分化。维生素 D 还会影响免疫系统,VDR 在几种白细胞中表达,包括单核细胞和活化的 T 细胞和 B 细胞。[20][7])
除了 VDR 激活之外,还有一些其他作用机制。其中一个重要机制是它作为刺猬信号通路(一种参与形态发生的激素)的天然抑制剂的作用。[21][22][8][9]
维生素 D 最重要的作用之一是通过促进肠道中钙的吸收、通过增加破骨细胞数量来促进骨骼重塑、维持骨骼形成所需的钙和磷水平,以及使甲状旁腺激素正常发挥作用来维持血清钙水平,从而维持骨骼中的钙平衡。维生素 D 缺乏会导致骨矿物质密度降低,以及骨密度降低(骨质疏松症)或骨折风险增加,因为缺乏维生素 D 会改变人体中的矿物质代谢。[23][10]) 因此,尽管乍看起来可能有些矛盾,但维生素 D 对于正常的骨骼形成至关重要,尽管它是一种有效的骨骼重塑刺激剂。[24][11])
7.2.3 需求量
[edit | edit source]对于 50 岁以上成年人,建议每日维生素 D 摄入量为 400-800 国际单位 (IU)。对于 25-50 岁人群,建议每日维生素 D 摄入量为 400 国际单位 (IU)。为了维持健康的维生素 D 水平,您需要食用富含维生素 D 的食物,例如脂肪鱼、鸡蛋、牛奶和谷物。此外,每周 2-3 天,在阳光下照射 15 分钟,可以让您的身体通过皮肤吸收足够的维生素 D。
维生素 D 状态定义的变化
基于对生物标记物(如 PTH 和肠道钙吸收)以及功能性健康结果的研究,近年来,维生素 D 缺乏症的定义发生了巨大变化。1997 年,美国国家科学院 (IOM) 和美国儿科学会 (AAP) 将婴儿和儿童的维生素 D 缺乏症定义为血清 25(OH)D 水平低于 11 ng/mL[12],但现在低于 20 ng/mL 的水平被认为是缺乏 [4]。表 I 显示了基于血清 25(OH)D 水平的维生素 D 状态分类 [4]。IOM 最近发表了一篇关于钙和维生素 D 膳食参考摄入量的综述[13]。这篇综述表明,由于关于非骨骼健康益处的研究结果存在差异且结论不一致,目前尚无足够的证据建议更高的血清 25(OH)D 水平。它认为,大多数人群的益处与大约 20 ng/ml 的水平相关,使用更高的临界值会人为地增加维生素 D 缺乏症的患病率估计。这篇综述以骨骼健康为基础制定了膳食参考摄入量 (DRI)。迫切需要遵循这些关于维生素 D 状态的当前定义,因为儿科医生(和产科医生)因在解决患者亚最佳维生素 D 状态方面行动缓慢而受到指责。
| 维生素 D 状态 | 血清 25(OH)D 水平 (ng/ml) |
|---|---|
| 严重缺乏 | <=5 |
| 缺乏 | <=15 |
| 不足 | 15-20 |
| 充足 | 20-100 |
| 过量 | >100 |
| 中毒 | >150 |
参考文献
[edit | edit source]- ↑ Walter F., PhD. Boron (2003). "The Parathyroid Glands and Vitamin F". Medical Physiology: A Cellular And Molecular Approaoch. Elsevier/Saunders. p. 1094. ISBN 978-1-4160-2328-9.
- ↑ Adams JS, Hewison M (2010). "Update in Vitamin D". Journal of Clinical Endocrinology & Metabolism 95 (2): 471–8. doi:10.1210/jc.2009-1773. PMC 2840860. PMID 20133466.
- ↑ a b Invalid
<ref>tag; no text was provided for refs namedRiver - ↑ Bouillon R, Van Cromphaut S, Carmeliet G (2003). "Intestinal calcium absorption: Molecular vitamin D mediated mechanisms". Journal of Cellular Biochemistry 88 (2): 332–9. doi:10.1002/jcb.10360. PMID 12520535.
- ↑ Holick MF (2004). "Sunlight and vitamin D for bone health and prevention of autoimmune diseases, cancers, and cardiovascular disease". The American Journal of Clinical Nutrition 80 (6 Suppl): 1678S–88S. PMID 15585788.
- ↑ Puchacz E, Stumpf WE, Stachowiak EK, Stachowiak MK (February 1996). "Vitamin D increases expression of the tyrosine hydroxylase gene in adrenal medullary cells". Molecular Brain Research 36 (1): 193–6. doi:10.1016/0169-328X(95)00314-I. PMID 9011759.
- ↑ Vitamin D The Physicians Desk Reference. 2006 Thompson Healthcare.
- ↑ Sarkar FH, Li Y, Wang Z, Kong D (2010). "The role of nutraceuticals in the regulation of Wnt and Hedgehog signaling in cancer". Cancer Metastasis Reviews 29 (3): 383–64. doi:10.1007/s10555-010-9233-4. PMC 2974632. PMID 20711635.
- ↑ "Hedgehog signaling and Vitamin D". Medscape.com. 2009-12-18. Retrieved 2010-03-25.
- ↑ Bell TD, Demay MB, Burnett-Bowie SAM (April 2010). "The biology and pathology of vitamin D control in bone". Journal of Cellular Biochemistry 111 (1): 7–13. doi:10.1002/jcb.22661. PMID 20506379.
- ↑ American Academy of Periodontology 2010 In-Service Exam, question A-27
- ↑ Standing Committee on the Scientific Evaluation of Dietary Reference Intakes Institute of Medicine. Dietary Reference Intakes for Calcium, Phosphorus, Magnesium, Vitamin D, and Fluoride. Washington, DC: National Academy; 1997. 45. Gartner LM, Greer FR. Prevention of rickets and vitamin D deficiency: new guidelines for vitamin D intake. Pediatrics. 2003;111:908-10.
- ↑ Ross AC, Taylor CL, Yaktine AL, Del Valle HB. Dietary Reference Intakes for Calcium and Vitamin D. Committee to Review Dietary reference Intakes for Vitamin D and calcium. Food and Nutrition Board, Institute of Medicine 2010. The National Academies Press, Washington D.C.
- ↑ Rathi, N., & Rathi, A. (2011). Vitamin d and child health in the 21 st century. In N. Rathi (Ed.), From Rathi Children’s Hospital and Maternity Home, Akola; and *Seth GS Medical College and KEM Hospital, Parel; Mumbai 400 012; MS, India. (August ed., Vol. 48, p. 622). India: Indian Paediatrics.
• http://www.spine-health.com/conditions/osteoporosis/calcium-and-vitamin-d-requirements
维生素 D 可以通过两种方式获得,一是通过阳光照射,如前所述;二是通过食物。维生素 D 最初以 25-羟基维生素 D 的非活性形式存在,然后通过两个过程进行羟化,使其转化为人体可利用的形式。第一个羟化过程发生在肝脏,维生素 D 在这里转化为骨化三醇。第二个羟化过程主要发生在肾脏,它将维生素 D 激活为我们使用的激素,即活性维生素 D。确定人体需要多少维生素 D 的最佳方法是观察血清浓度。根据维生素 D 健康资料表,血清 25(OH)D 浓度是衡量维生素 D 状态的最佳指标(美国国立卫生研究院)。这种血清浓度代表了我们体内维生素 D 的状态,即我们从阳光和食物中吸收的维生素 D 量。它可以通过血液检测,帮助我们了解体内是否有足够的维生素 D 来执行某些功能,例如代谢功能。血清 25(OH)D 浓度以纳摩尔每升 (nmol/L) 报道。根据血清 25-羟基维生素 D [25(OH)D] 浓度与健康的关系表,任何水平高于 30 nmol/l 但低于 12 nmol/l 的情况会导致儿童佝偻病和成人软骨病。健康个体骨骼和整体健康的充足血清水平为 20-50 nmol/l(美国国立卫生研究院)。回到旧石器时代,裸猿假说应运而生。它表明,在我们不断暴露在阳光下的时期,我们体内所需的特定 25(OH)D 浓度被固定在我们的基因中。这种基因组通过达尔文的自然选择理论进行了优化。25(OH)D 水平出现在富含紫外线的环境中,现在可以在那些大部分时间在阳光下度过的人身上看到。似乎血清 25(OH)D 浓度受到我们失去毛发、获得衣物以及从游牧生活方式转变为定居生活方式的进化影响。
7.3.4 缺乏症
[edit | edit source]维生素D缺乏可能是由于摄入的富含维生素D的食物不足或阳光照射不足所致。当这种情况发生时,患佝偻病的可能性会增加。佝偻病是一种骨骼变软变弱并开始弯曲的疾病。最容易患维生素D缺乏症的人群包括:• 生活在阳光照射很少的地区的人• 在白天在室内工作• 素食者• 乳糖不耐受者• 不吃乳制品的人
佝偻病和软骨病是典型的维生素D缺乏症。在儿童中,维生素D缺乏导致佝偻病,导致骨骼畸形。在成年人中,维生素D缺乏会导致软骨病,除了骨骼脆弱外,还会导致肌肉无力。可能患有维生素D缺乏症的高危人群包括老年人、肥胖者、纯母乳喂养的婴儿以及阳光照射有限的人。此外,患有脂肪吸收不良综合征(如囊性纤维化)或炎症性肠病(如克罗恩病)的人也有风险。
维生素D缺乏症在非裔美国人和拉丁美洲人中更为常见;(黑色素会降低皮肤对阳光照射产生维生素D的能力。一些研究表明,皮肤较深的老人患维生素D缺乏症的风险很高)。其他情况是当肾脏无法将维生素D转化为其活性形式时,随着年龄的增长,肾脏转换维生素D为其活性形式的能力下降,从而增加了患维生素D缺乏症的风险。
维生素D是一种脂溶性维生素,其在体内的合成取决于多种因素,如纬度、大气污染、衣物、皮肤色素沉着以及阳光照射的持续时间和时间。粮农组织/世卫组织专家协商会5指出,在世界上大多数纬度在北纬42°和南纬42°之间的地区,阳光充足。这有利于人体在皮肤中从皮下脂肪中存在的7-脱氢胆固醇内源性产生维生素D。每天在上午10点到下午2点之间(因为在此期间紫外线B射线的传输量最大)将手臂和脸部的皮肤暴露在阳光下 30 分钟,无需使用防晒霜,即可避免维生素D缺乏。[1]
为了治疗维生素D缺乏症,你需要通过饮食补充维生素D,并进行阳光照射,或者服用补充剂。如果这个问题没有及时解决,患佝偻病、骨痛、畸形和生长受损的可能性会更大。
美国国家科学院的维生素D补充剂建议包括:从出生到 50 岁,每天 200 IU 维生素 D;51 岁到 70 岁,每天 400 IU;70 岁及以上,每天 600 IU。这些建议假设有一定的阳光照射和食物中的维生素D摄入,不足以治疗维生素D缺乏症。
7.2.5 毒性
[edit | edit source]毒性
维生素D中毒,也称为维生素D过量症,是指体内维生素D过多。维生素D存在于食物中,通常在皮肤中使用阳光合成。然而,维生素D中毒通常是由于服用高剂量的维生素D补充剂造成的。这主要是由于身体能够调节阳光产生的维生素D水平,而且维生素D只天然存在于极少数食物中。[25]
早期症状包括呕吐、恶心和体重减轻。过量的维生素D后来会导致钙化。钙化是指血液中钙的积聚,会导致组织、骨骼和血管系统中钙含量过高。钙化还会导致高血压和肾脏损伤,因为肾脏试图通过排尿排出过量的钙。[26] 毒性的诊断包括每周测量血清Ca水平,然后在后期每月测量一次。一旦诊断确定,将停止服用维生素D,并用静脉注射生理盐水进行治疗。骨吸收抑制剂,如皮质类固醇或双膦酸盐,也将用于降低血液中的钙水平。[27]
当有人摄入了过量的维生素D时,会导致血液中钙含量过高,进而会导致肾脏损伤。这会带来许多症状,包括:• 便秘• 食欲不振• 呕吐• 脱水• 疲劳
可以通过一些检测来确认诊断,例如血液检测和X射线。
维生素D的评估
过去,血清维生素D的测量受到方法学差异(问题)的限制17-19。随着125I放射免疫分析(RIA)用于估计血清25-羟基维生素D[25(OH)D]的出现,方法学差异已消失(消失),允许对值进行实验室间比较。[目前可用的分析方法对25(OH)D2和25(OH)D3都有特异性抗体,因此使用25(OH)D分析方法这一术语。实验室通常估计25(OH)D水平,而不是25(OH)D2或25(OH)D3]。18-24 这些进展受到对维生素D缺乏症和维生素D缺乏症定义不当的限制。[2]
血清25(OH)D的评估需要进行血液检测,这不是医疗保健提供者常规进行的程序。维生素D水平正在下降(Looker等人,2008),因此在适当的时候实施检测非常重要。**一种非侵入性筛查工具可以帮助确定是否需要进行血清25(OH)D检测,但目前还没有经过验证、可靠、多项维生素D筛查工具,适用于在社区健康/保健环境中进行自我管理。**[3]
唯一的方法是停止摄入过量的维生素D,并去看你的全科医生,因为他们可以建议进一步的治疗步骤。
参考文献
[edit | edit source]- ↑ Londhey, V. (2011). Vitamin d deficiency: Indian scenario. In V. JAPI (Ed.), (Vol. 59, p. 695). India: JAPI. doi:www.japi.org
- ↑ Harinarayanan, C., & Shashank, R. J. (2009). Vitamin d status in india – its implications and remedial measures. In C. JAPI (Ed.), JAPI-review article (Vol. 57, pp. 41). India: JAPI. doi:www.japi.org
- ↑ Looker, A. C., Pfeiffer, M., Lacher, D. A., Schleicher, R. L., Picciano, M. F., & Yetley, E. A. (2008). Serum 25-hydroxyvitamin D status of the US population: 1988–1994 compared with 2000-2004. American Journal of Clinical Nutrition, 88, 1519–1527.
1. Harinarayanan, C., & Shashank, R. J. (2009). Vitamin d status in india – its implications and remedial measures. In C. JAPI (Ed.), JAPI-review article (Vol. 57, pp. 40–49). India: JAPI. doi:www.japi.org
2. Londhey, V. (2011). Vitamin d deficiency: Indian scenario. In V. JAPI (Ed.), (Vol. 59, p. 695). India: JAPI. doi:www.japi.org
3.Standing Committee on the Scientific Evaluation of Dietary Reference Intakes Institute of Medicine. Dietary Reference Intakes for Calcium, Phosphorus, Magnesium, Vitamin D, and Fluoride. Washington, DC: National Academy; 1997.
4. Gartner LM, Greer FR. Prevention of rickets and vitamin D deficiency: new guidelines for vitamin D intake. Pediatrics. 2003;111:908-10.
5. Ross AC, Taylor CL, Yaktine AL, Del Valle HB. Dietary Reference Intakes for Calcium and Vitamin D. Committee to Review Dietary reference Intakes for Vitamin D and calcium. Food and Nutrition Board, Institute of Medicine. 2010. The National Academies Press, Washington D.C
6. Rathi, N., & Rathi, A. (2011). Vitamin d and child health in the 21 st century. In N. Rathi (Ed.), From Rathi Children’s Hospital and Maternity Home, Akola; and *Seth GS Medical College and KEM Hospital, Parel; Mumbai 400 012; MS, India. (August ed., Vol. 48, p. 622). India: Indian Paediatrics.
7. Looker, A. C., Pfeiffer, M., Lacher, D. A., Schleicher, R. L., Picciano, M. F., & Yetley, E. A. (2008). Serum 25-hydroxyvitamin D status of the US population: 1988–1994 compared with 2000-2004. American Journal of Clinical Nutrition, 88, 1519–1527.
8. Dorland's Illustrated Medical Dictionary, under Vitamin (Table of Vitamins)
9. History of Vitamin D University of California, Riverside, Vitamin D Workshop.
10. Crissey SD, Ange KD, Jacobsen KL, Slifka KA, Bowen PE, Stacewicz-Sapuntzakis M, Langman CB, Sadler W, Kahn S (2003). "Serum concentrations of lipids, vitamin D metabolites, retinol, retinyl esters, tocopherols and selected carotenoids in twelve captive wild felid species at four zoos". The Journal of nutrition 133 (1): 160–6. PMID 12514284.
11. Hume EM, Lucas NS, Smith HH (1927). "On the Absorption of vitamin D from the Skin". Biochemical Journal 21 (2): 362–367. PMC 1251921. PMID 16743844.
12.C. Claiborne Ray (2005-05-17). "Sunshine Vitamin D". The New York Times. Retrieved 2013-03-08.
13. Holick MF (March 1995). "Environmental factors that influence the cutaneous production of vitamin D" (PDF). The American Journal of Clinical Nutrition 61 (3 Suppl): 638S–645S. PMID 7879731.
14. Yahav S,Buffenstein R(1993)。“补充胆钙化醇会改变地下居民裸鼠(Heterocephalus glaber)在以胡萝卜为食时的肠道功能并提高消化率”。《英国营养学杂志》第69卷(1):233-41。doi:10.1079/BJN19930025。PMID 8384476。
15. Stout SD,Agarwal SC(2003)。骨质流失和骨质疏松症:人类学视角。纽约:克鲁维尔学术/普伦姆出版社。ISBN 0-306-47767-X。
16. Adams JS,Hewison M(2010)。“维生素D更新”。《临床内分泌与代谢杂志》第95卷(2):471-8。doi:10.1210/jc.2009-1773。PMC 2840860。PMID 20133466。
17. Bouillon R,Van Cromphaut S,Carmeliet G(2003)。“肠道钙吸收:分子维生素D介导的机制”。《细胞生物化学杂志》第88卷(2):332-9。doi:10.1002/jcb.10360。PMID 12520535。
18. Holick MF(2004)。“阳光和维生素D促进骨骼健康,预防自身免疫性疾病、癌症和心血管疾病”。《美国临床营养学杂志》第80卷(6期补充):1678S-88S。PMID 15585788。
19. Puchacz E,Stumpf WE,Stachowiak EK,Stachowiak MK(1996年2月)。“维生素D增加肾上腺髓质细胞中酪氨酸羟化酶基因的表达”。《分子脑研究》第36卷(1):193-6。doi:10.1016/0169-328X(95)00314-I。PMID 9011759。
20. 维生素D[失效链接] 医师案头参考。2006 Thompson Healthcare。
21. Sarkar FH,Li Y,Wang Z,Kong D(2010)。“营养保健品在癌症中调节Wnt和Hedgehog信号通路中的作用”。《癌症转移评论》第29卷(3):383-64。doi:10.1007/s10555-010-9233-4。PMC 2974632。PMID 20711635。
22.“Hedgehog信号通路和维生素D”。Medscape.com。2009-12-18。检索于2010-03-25
23. Bell TD,Demay MB,Burnett-Bowie SAM(2010年4月)。“骨骼中维生素D控制的生物学和病理学”。《细胞生物化学杂志》第111卷(1):7-13。doi:10.1002/jcb.22661。PMID 20506379。
24. 美国牙周病学会2010年在职考试,问题A-27
25. Zeratsky,K.(2015)。维生素D中毒:什么是维生素D中毒,我应该担心我服用补充剂吗?。Mayo Foundation: 健康生活方式。
26. Ross,C.,Taylor,L.,& Yaktine,L.(2011)。钙和维生素D的膳食参考摄入量。国家生物技术信息中心,6。
27. Johnson,L.(2014)。维生素D:维生素D中毒。Merick Manual Professional Version。
- http://www.telegraph.co.uk/health/healthnews/8443773/The-best-natural-sources-of-Vitamin-D.html
- http://www.nhs.uk/Conditions/vitamins-minerals/Pages/Vitamin-D.aspx
- http://www.mayoclinic.com/health/vitamin-d/NS_patient-vitamind
- http://www.sfgate.com/health/article/Vitamin-D-deficiency-and-how-to-avoid-it-4196666.php
- http://jop.ascopubs.org/content/6/2/97.full
- http://www.bocsci.com/vitamin-d5-cas-71761-06-3-item-453668.html
