结构生物化学/相图
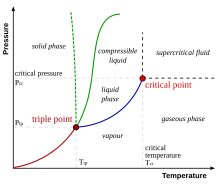
相图是一个图表,它有助于定义物质处于固态、液态和气态时的条件。图表的三个边界线表示相之间的平衡关系:熔化曲线、汽化曲线和升华曲线。图表上还有两个不同的点:三相点和临界点。为了更好地定义这些术语,可以观察图片图表。红线是固态到气态之间的转变,也称为升华曲线。绿线是固态到液态的转变,也称为熔化曲线。蓝线是液态到气态的转变,称为汽化曲线。三条线相交的点是三相点。在这个温度和压力下,三个相:固态、液态和气态可以共存。临界点是物质能够观察到的蒸汽/液体平衡的最高压力和温度条件。
任何超过最高压力和温度的条件都会变成一个没有明确相界限的区域。通常,当汽化来自恒定 T 下的减压时,相被认为是液体,如果冷凝来自恒定 T 下的降温,则相同情况适用于气体。由于此过程不能应用于任何一种情况,因此超过最高 P 和 T 的区域可以被认为是超临界的,并且是流体区域。
超临界流体被定义为高于其临界温度 (Tc) 和临界压力 (Pc) 的物质。临界点表示物质以蒸汽和液体平衡状态存在的最高温度和压力。超临界流体是高度压缩的气体,以一种引人入胜的方式结合了气体和液体的特性。超临界氙气、乙烷和二氧化碳等流体在合成化学和分析化学中都提供了各种不寻常的化学可能性。超临界流体对大多数溶质的溶解能力类似于轻质烃。然而,氟化化合物通常比在烃中更易溶于 scCO2。这种溶解度提高对于聚合反应很重要。

虽然相图通常被视为显示物质在特定条件下的状态的图,但这种简单的工具可以用于分析其他复杂材料。例如,从相图中获得的信息可用于讨论蛋白质晶体学。该图表示蛋白质晶体学所需的蛋白质和沉淀剂浓度。红线称为溶解度线,它将过饱和条件与未饱和条件明显分开,而过饱和条件是蛋白质结晶所需的条件。相图的过饱和部分包含三个部分:亚稳态、不稳定和沉淀。
亚稳态-这里的晶体可以从晶种长大,但不能成核。蛋白质和沉淀剂浓度较低,聚集事件较少。这个区域表示通常结晶发生速度太慢的浓度。
不稳定-这里的晶体也可以从晶种长大,但它们可以成核。蛋白质和沉淀剂浓度较高,聚集事件更多。这个区域也称为成核区或结晶区,更有利于晶体的形成。
沉淀-蛋白质通常以聚集体或沉淀物形式出现,不适用于晶体学。该图的这一部分显示了不太有利的条件,因为聚集和沉淀比结晶发生得快得多。
成核:创建核心的过程。
聚集:蛋白质的团聚或聚集。
相图和蛋白质结晶之间的联系是溶解度曲线(红线)的位置。如前所述,晶体只能在过饱和溶液中形成,了解溶解度曲线的位置可以促进晶体生长,用于 X 射线晶体学。虽然需要晶体来确定溶解度曲线,但通过各种试验可以找到适合晶体形成的浓度。通过这种数据积累,晶体可以用作优化蛋白质结晶条件的指南。
该相图也被使用,因为它揭示了溶液中多种组分之间的相互作用。此类相互作用的例子是定义蛋白质之间吸引力的液-液相分离 (LLPS),这是蛋白质结晶的必要特征。这种吸引力在 LLPS 中得到了很好的定义。可以从相图中提取的其他数据包括焓(来自 LLPS)和熵(来自溶解度曲线)在液态和固态中的蛋白质。此外,添加剂可以改变相图的曲线,从而提供有关添加剂效应以及它如何与蛋白质分析物相互作用的数据。它也可以用于预测蛋白质结晶所需条件,这对于结晶过程来说是理想的,减少了试错,并提高了结晶率。
向蛋白质溶液中添加沉淀剂的结果是形成液滴。这些液滴有时被称为油或凝聚体,可以在改变温度、pH 值和其他溶液条件变化时观察到。液滴通常含有高浓度的蛋白质,当受到更高的力(重力)影响时,液滴会从溶液的其余部分分离出来。其结果是溶液中的两个液相。整个过程称为液-液相分离。LLPS 很有用,因为高浓度的蛋白质有助于将饱和度提高到过饱和状态,从而增加了结晶率。
