有机化学/环烷烃
环烷烃是一种具有环或环状结构的常规烷烃。例如环己烷,它是一个由 6 个碳原子组成的环,每个碳原子连接到 2 个氢原子 (C6H12)。
我们在本书的烷烃单元中简要讨论了环烷烃,但在本单元中,我们将更详细地介绍环烷烃和环烯烃。这些结构有一些独特的性质,因此值得特别关注。
由于环状结构,环烷烃不具备普通烷烃所具有的旋转自由度。立体化学在运动的限制以及在某些情况下反应的限制方面起着非常重要的作用。这些限制往往更多地是由于环状结构本身,而不是由于此类烷烃中缺乏旋转自由度。
一个很好的例子是对E2消除反应的限制,我们将在本书的后面部分讨论。

上面显示的前四个简单环烷烃的图像表明,每个碳原子连接了 2 个氢原子。如您所见,另外 2 个键连接到相邻的碳原子。虽然这些形状显示了基本的二维、自上而下的形状,但只有环丙烷和环丁烷的所有碳原子都在同一平面上。环戊烷和环己烷以及更高环烷烃都具有三维几何形状。环己烷尤为重要,我们将在后面单独讨论。

更常见的是,环烷烃,像许多其他有机结构一样,被绘制成不标记碳原子和氢原子。环戊烷和环己烷(见上文)通常分别绘制成五边形和六边形。
环烷烃的命名类似于烷烃。最小的环烷烃是“环丙烷”,因此您可以想象,这是一个由 3 个碳原子组成的环。如果环烷烃上的碳原子数量多于其任何取代基(即连接到环烷烃上的碳原子上的碳链)上的碳原子数量,则基本名称前缀为“环”,其余名称与具有相同碳原子数量的烷烃相同。

如果,如上图所示,环烷烃的碳原子数量少于它连接的碳链的碳原子数量,则最长的碳链是主要的,而环状部分接收取代基“-yl”后缀并在主要名称前添加前缀。因此,名称 1-乙基丁基环戊烷虽然在技术上是准确的描述,但不是正确的名称。

取代环烷烃中碳原子的编号相当简单。如果只有一个取代基,则为 1 碳。如果有多个取代基,则编号顺时针或逆时针进行,使得 1 之后的最低编号对应于取代基最少(或至少)的碳原子。我知道这听起来很棘手,所以我们来看一下左边的例子,3-氯-1,1-二甲基环己烷。具有氯键的碳原子是取代基最少的碳原子,因此它得到 1 之后的最低编号,而 1 则对应于最靠近具有多个取代基的碳原子的碳原子。因此,1 应用于甲基。取代基仍然按字母顺序排列,如第二个例子 2-溴-3-氯-1,1-二甲基环己烷所示。
具有 4 个单键的碳原子希望这些键处于 109.5° 的四面体角。1885 年,阿道夫·冯·拜耳提出,由于碳原子更喜欢这个角度,因此只有 5 元环和 6 元环才能形成。拜耳犯了一个错误,就是用二维思维来思考并假设所有环都是平面的。事实上,只有环丙烷和环丁烷是平面的,导致它们的键角分别为 60° 和 90°。但在一段时间内,人们认为这些较小的环烷烃无法合成,而超过 6 个碳原子的环烷烃会产生张力,因为它们的键角将远远超过 109.5° 的偏好角度。

在上图中,再次展示了前四个简单环烷烃,但这次显示了三维模型。请注意环戊烷是如何有 4 个碳原子在同一个平面上,而第 5 个碳原子稍微偏离平面,使其呈现出打开的信封形状。
事实上,大于 3 个碳原子的环具有减轻这种键张力的三维形状,但重要的是要注意键张力确实会影响稳定性。对于环丙烷和环丁烷,张力能约为 110 kJ/mol。环丁烷可以进入“褶皱”形式,略微减轻了一些扭转张力。环戊烷是非平面的,可以消除一些张力,只有大约 25 kJ/mol 的张力。环己烷由于其椅式构象,可以保持完美的四面体角,从而没有张力。随着环尺寸进一步增加,可以避免键角张力,但会引入一些重叠张力,反之亦然,因此会存在一些张力,但其中张力最大的,环壬烷,只有大约 50 kJ/mol 的张力。环张力在高达 13 个成员的环尺寸中普遍存在。之后,有足够的碳原子可以完全消除环张力。

但键角张力并不是环张力中唯一涉及的问题。扭转张力也是一个因素。当环中的氢键相互重叠时,就会产生额外的张力。在环丙烷的情况下,氢原子相互重叠,极大地增加了张力。事实上,这是环戊烷中大部分张力的原因。环戊烷的键角非常接近 109.5°,但由于其 4 个碳原子是平面的,因此存在扭转张力,使其不太稳定。从上图中可以看到,沿着平面上的 2 个键观察环戊烷,其中非平面碳原子最靠近我们,可以看到键的弯曲使氢原子能够稍微脱离重叠,从而在一定程度上减轻了扭转张力。
环己烷是最小的环,能够具有 109.5° 的键角并保持交错构象,使其没有张力。
环己烷有 3 种主要构象,即椅式、反椅式和船式。椅式构象没有键角张力、扭转张力或空间张力。然而,船式构象确实具有空间张力,因为船式前后的高点处的氢原子略微重叠。
待办事项
环己烷的不同构象在某些反应中会表现出不同的反应性。例如,E2 消除反应,我们将在本书的后面部分讨论,需要卤素原子和氢原子位于相邻的碳原子且彼此共面,或 180°(反式)。在具有多个取代基连接到其碳原子的环己烷中,氢原子和卤素原子可能位于相邻的碳原子,但永远不会共面,因此阻止反应发生。
在其他反应中,相邻取代基的空间位阻,例如相邻碳原子上的较大烷基,会阻止亲核试剂攻击所需的位点。出于这些以及其他原因,了解反应物的三维几何形状和结构以及正在发生的反应机理非常重要。
待办事项
在某些化合物中,两个或多个环融合在同一个分子中。这可能发生在脂肪族和芳香族化合物中。
如果两个环在一个碳原子上相遇,并且该碳原子是两个环的一部分,则该化合物被称为螺环化合物。由于碳原子周围四个配体的常规四面体键合,两个环大致(但并非完全)彼此垂直。
如果两个环在两个或多个碳原子上桥接,则碳原子形成桥的一部分,并且该化合物是双环烷烃(对于两个环)或多环烷烃(对于三个或更多环)。
芳香族双环化合物是萘 (C10H8),它是由两个苯环融合在碳-碳键上形成的。脂肪族(非芳香族)双环化合物是十氢萘 (C10H18),正式名称为十氢萘,它是由两个环己烷环融合在 C-C 键上形成的。
双环烷烃环系统由三个部分组成
- 较长的碳链 (a)
- 较短的碳链 (b)
- 碳-碳桥 (c)
注意 始终成立。
双环环的命名方式如下,根据碳的总数进行命名
- 双环[a.b.c]烷
在此公式中,将 [a.b.c] 替换为碳链的长度,并将“烷”替换为碳的总数(庚烷、辛烷、壬烷等)。
一个著名的双环化合物例子是降冰片烷(见下图)。降冰片烷的正式名称是双环[2.2.1]庚烷。桥的左侧有两个碳,桥的右侧有两个碳,桥本身有一个碳。因此,括号中的数字为 [2.2.1]。请注意,桥底部的两个碳没有计入括号中。
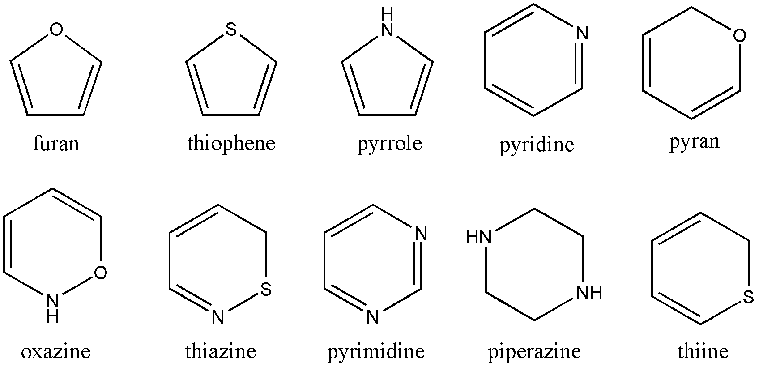
杂环化合物是指环中包含碳以外的原子的环状化合物。上图仅显示了一些单环杂环化合物。所示的只是 5 元和 6 元环。还有更小和更大的环,以及多环杂环。
杂环化合物在有机化学中起着重要作用,由于它们的电子构型与碳不同,因此它们的反应方式不同于碳环,并且彼此之间也不同。在本书的后面,我们将讨论几种在有机化学中非常常用的特定杂环化合物,并讨论它们的各自特性。
现在,重要的是要知道什么是杂环化合物。


