AP 化学/电化学
氧化数只是每个化合物中单个元素的电荷。要找到某个东西的氧化数,需要记住一些规则
任何纯净的、电荷为 0 的物种,其氧化数为 0
示例方程
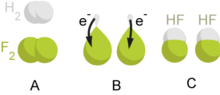
还原:当离子/元素获得电子时( 被还原为 )
氧化:当离子/元素失去电子时( 被氧化为 )
还原剂:将电子传递给另一个离子/元素的离子/元素( 是对 的还原剂)
氧化剂:从另一个离子/元素中获取电子的离子/元素( 是对 的氧化剂)
在氧化还原反应中,电子会发生转移。这些转移会导致两种金属之间产生标准电池电势(以伏特为单位测量)。作为 AP 化学学生,你应该能够使用标准还原电势表来计算标准电池电势。该表格提供了每个元素/化合物的标准还原电势,即将 1 摩尔离子还原为还原态(它可以变成另一种离子或金属的纯形式)所需的电势伏特数。要找到标准电池电势,你需要找到被还原元素的还原电势和被氧化元素的氧化电势。氧化电势可以通过改变表格中找到的还原电势的符号来确定( 的还原电势为 -4.10, 的氧化电势为 4.10)。找到被还原元素的还原电势和被氧化元素的氧化电势后,只需将这两个值加在一起即可得到标准电池电势。
安培、法拉第和库仑
[edit | edit source]在观察原电池时,你需要能够计算在给定时间内沉积的特定金属的质量。为此,你需要了解一些新的单位。
库仑:库仑是 6.241×1018 个电子的电荷。
法拉第:法拉第是表示电子摩尔的过时说法。
安培:安培表示每秒库仑。它测量流过导线的电流。
法拉第常数:它表示每摩尔电子有 96,500 库仑。
原电池
[edit | edit source]这是一个原电池
电池的组成部分
[edit | edit source]原电池包含几个不同的组件
- 阳极:金属被氧化的地方,电子被释放到导线中,导致固态金属阳极变成离子。
- 阴极:来自导线的电子被离子浴中的离子接收的地方,导致还原,将离子转化为固态金属。
- 盐桥:盐溶解在水中的地方,每个离子移动到阳极或阴极,平衡需要平衡的任何电荷。阴离子移动到阳极,阳离子移动到阴极。盐桥中的盐必须是一种盐,如果阴离子与两种金属的离子结合,该化合物仍将保持溶解状态,不会固化。
- 金属离子浴:金属被氧化时变成离子后所在的溶液。也是还原后的离子固化并变成固态金属的地方。
- 导线:电子从阳极流向阴极的路径。
工作原理
[edit | edit source]根据标准还原电势表,还原电势较高(或氧化电势较低)的原电池将是阴极,另一种金属将是阳极。阳极中的电子被氧化,通过导线传递到阴极。这就是电压的确定方式,通过测量导线中电子的电流。
确定金属的生成质量
[edit | edit source]有了这些信息,我们需要弄清楚在给定安培数和时间的情况下,原电池中沉积了多少质量。让我们来看一个示例问题。
电解 溶液,电流为 ,持续时间为 ,可以生成多少克汞?
这里,我们给出了三个重要的信息。
- 电流为
- 持续时间为
第一条信息告诉我们如何建立净离子半反应。在这些类型的反应中,将有两种金属发生反应,一种氧化,一种还原。在本例中,我们实际上只需要关心还原反应,因为我们正在寻找汞的固体克数,而还原是产生固体汞的地方。
(注意:你可能遇到一个问题说“镀出”。这与“产生”的意思相同。)
为了建立我们的还原半反应,我们需要知道被还原金属的氧化值(基本上是指金属变成离子时,它的电荷是多少)。过渡金属具有两种或多种氧化态,但通常可以安全地使用最常见的一种(通常是 2+)。对于汞,本例中的氧化态是 2+。因此,我们的反应如下
有了这个方程式,我们现在知道了所有需要的摩尔比。让我们开始通过使用其他两条信息来设置转换因子。
由于安培是 所以需要将小时转换为秒,以便单位能够抵消。然后,使用法拉第常数得到电子摩尔数,然后将其乘以摩尔比,再乘以摩尔质量。
了解如何做这类问题,也了解如何从镀出的克数转换为时间等等。
电解池
[edit | edit source]
这与原电池相反。在这种类型的电池中,将一定的电压施加到一池液体上,可以是盐的熔融形式,也可以是溶解在水中的盐。这一次,人们是在向系统中添加能量,这意味着标准电池电位将为负。这种电流进入离子/熔融盐,基本上将它们分离出来,为你提供你正在使用的任何物质的纯净形式。“阳极”是具有较低氧化电位的金属,“阴极”具有较低的还原电位。这主要用于提纯金属和从盐中提取纯净物质。

















