结构生物化学/核酸/DNA/DNA 结构
脱氧核糖核酸 (DNA) 储存特定蛋白质合成信息。DNA 以 脱氧核糖 为其糖。 DNA 由磷酸基团、糖和 含氮碱基 组成。 DNA 的结构是一种螺旋状的双链大分子,碱基突向分子内部。这两条链的序列始终互补。在 DNA 复制(遗传的主要来源)过程中,一条链作为另一条链形成的模板。 DNA 的这一独特特征为生命连续性提供了一种机制。DNA 的结构是由罗莎琳德·富兰克林发现的,她使用 X 射线晶体学研究遗传物质。她获得的 X 射线照片揭示了 DNA 的物理结构为螺旋。
DNA 具有双螺旋结构。外边缘由交替的脱氧核糖糖分子和 磷酸基团 形成,构成糖磷酸骨架。这两条链以相反的方向延伸,一条从 3' 到 5' 方向,另一条从 5' 到 3' 方向。 含氮碱基 位于螺旋结构内侧,就像“梯子的横档”一样,这是由于疏水效应,并由氢键稳定。
| 含氮碱基 | 核苷 | 脱氧核苷 |
|---|---|---|
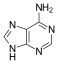 腺嘌呤 |
 腺苷 A |
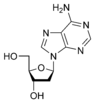 脱氧腺苷 dA |
 鸟嘌呤 |
 鸟苷 G |
 脱氧鸟苷 dG |
 胸腺嘧啶 |
 5-甲基尿苷 m5U |
 脱氧胸腺嘧啶 dT |
 尿嘧啶 |
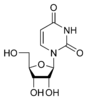 尿苷 U |
 脱氧尿苷 dU |
 胞嘧啶 |
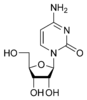 胞苷 C |
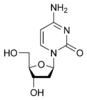 脱氧胞苷 dC |
这两条链以相反的方向延伸形成双螺旋。这些链通过氢键和疏水相互作用保持在一起。H 键形成于反平行链的碱基对之间。第一条链中的碱基只与第二条链中的特定碱基形成 H 键。这两个碱基形成一个碱基对(H 键相互作用,使链保持在一起并形成双螺旋结构)。 DNA 中的碱基对是 腺嘌呤-胸腺嘧啶 (A-T) 和 胞嘧啶-鸟嘌呤 (C-G)。这种相互作用使我们理解,含氮碱基位于 DNA 双螺旋结构内部,而糖和磷酸基团位于双螺旋结构外部。
由碱基和糖组成的成分称为核苷。 DNA 包含脱氧腺苷(脱氧核糖与 腺嘌呤 相连)、脱氧鸟苷(脱氧核糖与 鸟嘌呤 相连)、脱氧胞苷(脱氧核糖与 胞嘧啶 相连)和脱氧胸腺嘧啶(脱氧核糖与 胸腺嘧啶 相连)。碱基与糖之间键的连接称为 β-N-糖苷键。在 嘌呤 中,这发生在 N-9 和 C-1' 之间,在 嘧啶 中,这发生在 N-1 和 C-1' 之间。核苷和磷酸基团构成核苷酸。脱氧核糖核苷的脱氧核糖与磷酸基团之间的键是 3'-5' 磷酸二酯键。
位于双螺旋内部的碱基是堆积的。堆积碱基通过范德华力相互作用。虽然范德华相互作用的能量相对较小,但在螺旋结构中,大量的原子交织在一起进行这种相互作用,能量的净总和相当大。两个相邻碱基之间垂直于主轴的距离是 3.4 Å。 DNA 结构是重复的。每转十个碱基,也就是说结构在 34 Å 后重复,因此每个碱基的旋转角度为 36°。双螺旋的半径约为 10 Å。
区分核苷和脱氧核苷的简单方法是糖单元中与 C-2 相连的原子。如果结构是脱氧核苷,则 C-2 带有两个氢。如果是核苷,则 C-2 带有一个氢和一个羟基,其中羟基朝南。
如果发生以下情况,DNA 结构可能会发生变化
1. 存在不同的脱氧核糖构象
2. 如果磷酸脱氧核糖骨架中相邻键之间存在旋转
3. 围绕 C-1'N=糖苷键的自由旋转 (syn/anti)[1]
有两种类型的核酸,核糖核酸 (RNA) 和 脱氧核糖核酸 (DNA)。回想一下,核苷是碱基 + 糖。核苷酸由碱基 + 糖 + 磷酸组成。脱氧核苷酸中的“脱氧”前缀是用于 DNA 的命名法。当它用于 RNA 的命名法时,采用术语核糖核苷酸,换句话说,糖单元上的 C-2 具有 -OH 基团(与脱氧不同,脱氧的 C-2 具有 2 个氢)。使用符号来简化名称。例如,ATP(RNA 的前体)。前面的“A”表示碱基是 腺嘌呤,“T”表示三磷酸。另一方面,AMP 也具有 腺嘌呤,但 M 表示糖与单个磷酸基团结合。最后,在 dAMP 中,“d”表示它是 2'-脱氧核糖,而仅仅 AMP 表示它是核糖核苷酸。简而言之,DNA 的四个核苷酸单位称为脱氧腺苷酸、脱氧鸟苷酸、脱氧胞苷酸和胸腺嘧啶酸。
核酸的一级结构是指其共价结构和核苷酸序列。确定 DNA 结构最重要的部分之一来自埃尔温·查伽夫及其同事在 20 世纪 40 年代末的研究。他们发现,不同生物体的 DNA 中的四种核苷酸碱基数量不同,并且某些碱基的数量密切相关。他们得出以下关于 DNA 结构的结论:

1. DNA 的碱基组成通常因物种而异。
2. 从同一物种的不同组织中分离得到的 DNA 样本具有相同的碱基组成。
3. 给定物种中 DNA 的碱基组成不会随时间、营养状态或环境而改变。
4. 在所有细胞 DNA 中,无论物种如何,腺嘌呤残基的数量等于胸腺嘧啶残基的数量 (A=T),鸟嘌呤残基的数量等于胞嘧啶残基的数量 (G=C)。
后来在 1953 年,罗莎琳德·富兰克林和莫里斯·威尔金斯使用了一种强大的 X 射线衍射技术,称为 X 射线晶体学,推断出 DNA 的结构。通过 X 射线晶体学 方法产生的照片实际上不是分子照片,但是 X 射线通过结晶的 DNA 衍射(偏转)时产生的斑点和污点。晶体学家使用数学方程式将这些斑点模式转换为有关 DNA 三维形状的信息。富兰克林和威尔金斯发现,DNA 分子是螺旋形的,沿其长轴有两个周期性,一个主要的周期为 3.4 埃,另一个次要的周期为 34 埃。

沃森和克里克后来根据他们从威尔金斯和富兰克林的 X 射线衍射照片中提取的数据建立了 DNA 模型。
http://37days.typepad.com/37days/images/2008/03/02/franklin20dna20photo.jpg
他们解释了 X 射线照片上斑点的模式,这意味着 DNA 由两条链组成,呈螺旋形。最终,沃森和克里克根据 X 射线照片的衍射模式制定了 DNA 结构,并获得了今天仍然被接受的令人难以置信的见解。在这个结构中,他们提出两条方向相反的螺旋状 DNA 链缠绕在同一个轴上,形成右手双螺旋。亲水主链由交替的脱氧核糖糖和 磷酸 基团的磷酸二酯键形成,这些主链位于螺旋外部,被水环境包围。每个脱氧核糖糖的呋喃糖环处于 C-2' endo 构象。两条链的 嘌呤 和 嘧啶 碱基堆叠在双螺旋内部,并通过范德华相互作用稳定。
双螺旋的直径为 10 埃。双螺旋中一条链上的每个相邻碱基相距 3.4 埃。每 10 个碱基对构成螺旋的 360 度旋转,螺旋的长度由每 10 个碱基对的 34 埃决定。


DNA 分子是不对称的,这种性质在 DNA 复制 和转录过程中至关重要。双链 DNA 分子由两条互补但分离的链组成,通过氢键网络相互交织成螺旋状。虽然右手螺旋和左手螺旋都属于允许的构象,但右手螺旋在能量上更有利,因为侧链和主链之间的空间位阻更小。DNA 的方向由磷酸基团和脱氧核糖糖基团沿 DNA 主链的排列决定。DNA 的一个末端以 3'-OH 基团终止,而另一个末端以 5'-磷酸基团终止。所有 DNA 序列通常从 5' 末端到 3' 末端书写。在双螺旋形成中,互补的 DNA 链以相反的方向定向。DNA 是一种相当刚性的分子:在生理条件下,DNA 在大约 50 纳米的长度尺度上弯曲,这大约是双螺旋直径的 20 倍。更重要的是,碱基的对齐可以指示 DNA 链的全局方向。对于 嘌呤 核苷酸 (A 和 G),最可能的角度大约为 88 度,而对于 嘧啶 (C 和 T),该角度大约为 105 度。
DNA 双螺旋通过两种主要力量保持在一起:螺旋内部互补碱基对之间的氢键以及范德华碱基堆积相互作用。
沃森和克里克发现,氢键连接的碱基对,G 与 C,A 与 T,是最适合 DNA 结构的碱基对。需要注意的是,G 和 C 之间可以形成三个氢键,但在 A 和 T 对中只能找到两个键。另一方面,A-T 对似乎会使双螺旋结构不稳定。这一结论得益于一个已知的事实,即在每个物种中,G 的含量等于 C 的含量,T 的含量等于 A 的含量。
以下是碱基对之间氢键的演示链接
http://chemmac1.usc.edu/java/bases/basepairs.html
构成 鸟嘌呤 (G) 和 胞嘧啶 (C) 连接的三个氢键因此改变了 DNA 的热熔解,这取决于碱基组成。随着碱基组成的变化,这种分子的熔点也会升高或降低。
变性和退火
紫外 (UV) 光可以检测碱基是堆叠还是非堆叠。DNA 结构 中堆叠的碱基有利于屏蔽光线,因此双螺旋 DNA 对紫外光的吸收远小于单链 DNA。这种特性被称为减色效应,即 DNA 分子双螺旋发射的颜色更少。
熔点 (Tm) 是 DNA 一半处于双链状态,一半处于单链状态的温度。Tm 在很大程度上取决于碱基组成。由于 G-C 碱基对由于氢键更多而更强,因此 G-C 含量高的 DNA 将具有比 A-T 含量更高的 DNA 更高的 Tm。
当热量作用于双链DNA时,每条单链最终都会分离(变性),因为碱基对之间的氢键被破坏。分离后,分离的链会自发地重新结合,再次形成双螺旋结构。这个过程被称为退火。
在生物系统中,变性和退火都会发生。解旋酶利用化学能(来自 ATP)破坏双链核酸分子的结构。DNA在实验室中重新结合的能力研究对于发现基因结构和表达至关重要。
复杂结构
从单链DNA中也可以形成复杂结构。当同一链内的互补序列配对形成双螺旋结构时,就会形成茎环结构。同一链内的碱基对之间会形成氢键。通常,这些结构包含错配的碱基,导致局部结构的不稳定。这种作用在更高阶的折叠中可能很重要,比如在三级结构中。
DNA在接近紫外光波长(~260 纳米)处强烈吸收。单链 DNA 比双链DNA吸收更多的紫外光。DNA在形成双链时,其紫外吸收会降低,这种特性是DNA稳定性的一个指标。随着光能的增加,其结构及其功能仍然保持完整,因为其结构受到的干扰很小。
观察到的DNA双螺旋相对于天然和变性形式的吸光度降低可以用以下事实来解释:双螺旋结构中含氮碱基的堆积不会使它们暴露在辐射中,因此它们能够吸收的辐射更少。含氮碱基的芳香性(特别是在嘌呤和嘧啶等环状结构中)解释了吸收峰位于 260 纳米的原因。
各种弱力共同作用,稳定DNA结构。
- 氢键,碱基之间的连接,尽管能量上很弱,但由于DNA分子中存在大量的氢键,因此能够稳定螺旋结构。
- 堆积相互作用,也称为碱基之间的范德华相互作用,很弱,但大量的这种相互作用有助于稳定螺旋的整体结构。
- 双螺旋结构通过疏水效应稳定,将碱基埋在螺旋的内部会增加其稳定性;将疏水性碱基聚集在螺旋的内部可以防止它们与周围的水接触,而更极性的表面,即亲水性头部暴露出来,并与外部水相互作用。
- 堆积的碱基对也通过范德华力相互吸引,单个范德华相互作用所对应的能量对整体DNA 结构的影响很小,但是,对所有原子对进行求和得到的净效应会产生显著的稳定性。
- 堆积也倾向于有利于骨架磷酸-糖的较硬的五元环的构象。
- 电荷-电荷相互作用- 指带负电荷的磷酸盐之间的静电(离子-离子)排斥,这可能是不稳定的,然而,存在 Mg2+ 和富含精氨酸和赖氨酸残基的阳离子蛋白,它们会稳定双螺旋结构。
含氮碱基是DNA聚合物的基础结构,DNA 聚合物的结构随连接的不同含氮碱基而变化。
含氮碱基可以在酮式和烯醇式之间互变异构。嘧啶(胞嘧啶、胸腺嘧啶、尿嘧啶(RNA))和嘌呤(腺嘌呤、鸟嘌呤)环体系的芳香性和它们富含电子的 -OH 和 -NH2 取代基使它们能够发生酮-烯醇互变异构。酮式互变异构体称为内酰胺,烯醇式互变异构体称为内酰亚胺。在 pH 7 时,内酰胺占主导地位。酮-烯醇互变异构是酮和烯醇之间的相互转换,涉及质子的移动和成键电子的转移,因此这种异构体属于互变异构现象。
酮-烯醇互变异构在 DNA 结构中很重要,因为磷酸烯醇丙酮酸的高磷酸转移势导致磷酸化合物被困在较不稳定的烯醇式中,而脱磷酸化导致酮式。碱基鸟嘌呤和胸腺嘧啶的稀有烯醇式互变异构体可能由于碱基配对特性的改变而导致突变。
双链DNA的两个链通过许多弱相互作用结合在一起,例如氢键、堆积相互作用和疏水效应。在这些作用中,碱基对之间的堆积相互作用是最重要的。碱基堆积相互作用的强度取决于碱基。对于 G-C 碱基对的堆积,强度最强,而对于 A-T 碱基对的堆积,强度最弱。疏水效应使碱基彼此堆叠。堆积的碱基对通过范德华力相互吸引,通常为 2 到 4 kJ/mol-1。此外,DNA中的碱基堆积有利于骨架磷酸-糖的相对刚性的五元环的构象。碱基堆积相互作用在很大程度上与堆积的碱基的同一性无关,对双螺旋结构的稳定性做出了主要贡献。
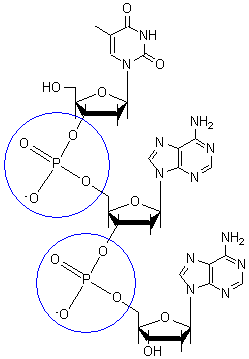
磷酸二酯键形成DNA的共价骨架。磷酸二酯键是在DNA中脱氧核糖的 3' 碳原子和 5' 碳原子之间形成的连接。
磷酸二酯键中的磷酸盐基团带负电荷。磷酸盐基团的 pKa 接近 0,因此它们在中性 pH(pH=7)下带负电荷。这种电荷-电荷排斥力迫使磷酸盐基团在DNA链的相反位置上,并被蛋白质(组蛋白)、金属离子(如镁)和多胺中和。
核苷酸构建块的三磷酸或二磷酸形式首先必须被分解,以释放驱动磷酸二酯键形成和核苷酸连接的酶促反应所需的能量。一旦单个磷酸或两个磷酸(焦磷酸盐)分解并参与催化反应,就会形成磷酸二酯键。
磷酸二酯键的水解由磷酸二酯酶催化,磷酸二酯酶是一种促进修复的酶,因此在修复DNA序列中发挥着重要作用。
DNA 比 RNA 更稳定的原因之一是 DNA 中没有 2'-OH 基团。2'C 上存在 OH 基团使 RNA 更容易发生反应。亲核试剂(碱基)可以拉出 H(当所有物质都处于正确的轨迹时),并且骨架的磷酸部分会重新排列,最终 P-O 键断裂,从而断开两个糖之间的连接位点。
大沟和小沟
互补核苷酸的碱基配对构成了DNA的二级结构。单链DNA可以参与互补碱基对之间的分子内碱基配对,因此也形成二级结构。腺嘌呤 (A)-胸腺嘧啶 (T) 和鸟嘌呤 (G)-胞嘧啶 (C) 之间的碱基配对是可能的,因为这些碱基对的大小相似。这意味着双螺旋结构内没有“凸起”或“间隙”。
双螺旋结构中碱基对的不规则排列会导致大分子失去功能。因此,如果结构出现问题,就会发出信号,DNA修复机制会修复损伤。
由于DNA的双螺旋结构,该分子具有两个不对称的沟槽。一个沟槽比另一个沟槽小。这种不对称性是由磷酸基、糖基和碱基之间键的几何构型造成的,它迫使碱基以120度角而不是180度角连接。较大的沟槽称为主沟,发生在骨架相距较远时;而较小的沟槽称为次沟,发生在骨架彼此靠近时。
由于主沟和次沟暴露了碱基的边缘,因此可以利用这些沟槽来判断特定DNA分子的碱基序列。这种识别的可能性至关重要,因为蛋白质必须能够识别特定的DNA序列,以便在这些序列上结合,以实现身体和细胞的正常功能。正如您所料,主沟比次沟包含更多信息,允许DNA蛋白与碱基相互作用。这一事实使得次沟不太适合蛋白质结合。

以下特征代表了 A 型 DNA 结构的不同特征
1. 大多数 RNA 和 RNA-DNA 双链以这种形式存在
2. 比 B 型更短、更宽的螺旋。
3· 深而窄的主沟不易被蛋白质访问
4· 广泛而浅的次沟可被蛋白质访问,但信息量低于主沟。
5· 在低水浓度下有利的构象
6· 碱基对相对于螺旋轴倾斜,并从轴上移位
7· 糖构象 C3'-endo(在 RNA 中 2'-OH 抑制 C2'-endo 构象)
8· 右旋
9· 尺寸约为 26 埃
10· 每螺旋圈需要 11 个碱基对
11· 糖苷键构象为反式
正常DNA的双螺旋结构采用右手形式,称为 B 型螺旋。它约为 20 埃,具有 C-2' endo 糖构象。螺旋大约每 10 个碱基对旋转一圈(= 每重复 34 埃 / 每碱基 3.4 埃)。B 型 DNA 具有两个主要的沟槽,一个宽的主沟和一个窄的次沟。许多蛋白质在主沟的空间内相互作用,在那里它们与碱基形成序列特异性接触。此外,已知一些蛋白质通过次沟形成接触。
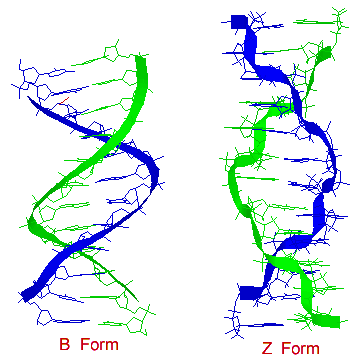
DNA序列可以从 B 型转变为 Z 型,反之亦然。Z 型DNA与 B 型结构有更根本的差异;最明显的区别是左手螺旋旋转。
Z 型约为 18 埃,每螺旋圈有 12 个碱基对,并且结构看起来更细长。DNA骨架呈现锯齿状。某些核苷酸序列比其他序列更容易折叠成左手 Z 型螺旋。突出的例子是嘧啶与嘌呤交替出现的序列,尤其是交替的 C 和 G 或 5-甲基-C 和 G 残基。为了在 Z 型 DNA 中形成左手螺旋,嘌呤残基翻转到顺式构象,与反式构象的嘧啶交替出现。在 Z 型 DNA 中,主沟几乎看不出来,而次沟则又窄又深。对于嘧啶,糖的构象为 C-2' endo,而对于嘌呤,糖的构象为 C-3' endo。
Z 型DNA的形成发生在基因转录过程中,发生在活跃转录基因的启动子附近的转录起始位点。在转录过程中,RNA 聚合酶的移动在转录位点上游诱导负超螺旋,在下游诱导正超螺旋。上游的负超螺旋有利于 Z 型 DNA 的形成;Z 型DNA的功能是吸收负超螺旋。在转录结束时,拓扑异构酶将 DNA 放松回 B 型构象。
DNA分子的三级结构是由 DNA 的两条链相互缠绕而成的。DNA 双螺旋可以在空间中排列,形成链的三级排列。
通常情况下,DNA 的 Lk 约为 25,这意味着它处于欠旋状态。然而,DNA 也可以被超螺旋化,形成两个“欠旋”,它是由负超螺旋组成的。这就像单链DNA 的两个“旋转”和没有超螺旋。这种螺旋和超螺旋旋转之间的相互转换在基因转录和调控中至关重要。
DNA 与组蛋白和非组蛋白结合形成染色质。由于DNA 中磷酸基团的负电荷,使其具有相对的酸性。这种负电荷与碱性组蛋白基团结合。
最近的研究表明,活跃转录区域以组蛋白的特定修饰模式为特征。对组蛋白修饰动力学的实验表明,甲基化、磷酸化和乙酰化之间存在显著的动力学差异。这表明这些修饰在基因表达模式中发挥着不同的作用。
组蛋白是蛋白质,DNA缠绕在其周围形成染色质。染色质的基本单位是核小体,由2个H2A、H2B、H3和H4组蛋白八聚体以及147个碱基对的DNA超螺旋构成。DNA的可及性受高级染色质结构的调节,这些结构可以通过核小体的堆积获得。人们认为,组蛋白分子的N端尾部有助于染色质功能,因为它介导核小体之间的相互作用,并参与将非组蛋白募集到染色质中。N端尾部引导与染色质结合因子的相互作用,这被认为是调节染色质结构的驱动力。然而,修饰可能以其他方式发生,例如观察到的核小体的展开或组装以及它如何参与基因调控。希望这能解释表观遗传的遗传(方框1),即个体之间表型差异不能仅仅归因于DNA差异,例如同卵双胞胎。
表观遗传的遗传是指基因活性的变化,这些变化不受DNA序列编码的影响。这些变化包括磷酸化、甲基化、ADP-核糖基化、SUMO化和泛素化。这些修饰可以根据它们在活跃基因或沉默基因中的出现被认为是激活的或抑制性的。研究表明,甲基化可能具有不同的结果,具体取决于组蛋白修饰的结合因子。核小体定位被发现对DNA序列有影响,可能有助于表观遗传的遗传。[2]
DNA的结构变异主要归因于
- 1) 脱氧核糖构象变化(共4种构象)
- 2) 磷酸脱氧核糖骨架中相邻键的旋转(C1-C3 和 C5-C6 之间)
- 3) C1'-N 糖苷键的自由旋转(导致syn或anti构象)
由于空间位阻,核苷酸中的嘌呤碱基在相对于脱氧核糖的两个稳定构象中受到限制,称为syn和anti。另一方面,嘧啶通常限于anti构象,因为糖和嘧啶C-2上的羰基氧之间存在空间干扰。
| A 型 | B 型 | Z 型 | ||
|---|---|---|---|---|
| 螺旋方向 | ||||
| 右手螺旋 | 右手螺旋 | 左手螺旋 | ||
| 直径 | ||||
| 26 埃 | 20 埃 | 18 埃 | ||
| 每螺旋周期的碱基对数 | ||||
| 11 | 10.5 | 12 | ||
| 每碱基对的螺旋上升 | ||||
| 2.6 埃 | 3.4 埃 | 3.7 埃 | ||
| 碱基相对于螺旋轴的倾斜角度 | ||||
| 200 | 60 | 70 | ||
| 糖的构象 | ||||
| C-3’ endo | C-2’ endo | 嘧啶为C-2’ endo,嘌呤为C-3’ endo | ||
| 糖苷键构象 | ||||
| Anti | Anti | 嘧啶为Anti,嘌呤为Syn |
Campbell and Reese's Biology, 7th Edition
Nelson and Cox's Lehninger Principles of Biochemistry, 5th Edition





